
【题目】某实验小组为探究ClO﹣、I2、SO ![]() 在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下: 实验①:在淀粉KI溶液中加入少量NaClO溶液,并加入少量的稀H2SO4 , 溶液立即变蓝;
在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下: 实验①:在淀粉KI溶液中加入少量NaClO溶液,并加入少量的稀H2SO4 , 溶液立即变蓝;
实验②:向实验①的溶液中加入4L 0.5mol/L的Na2SO3溶液,发生反应如下
SO ![]() +I2+H2O→SO
+I2+H2O→SO ![]() +I﹣+H+(未配平),恰好完全反应.
+I﹣+H+(未配平),恰好完全反应.
(1)以上实验说明,在酸性条件下ClO﹣、I2、SO42﹣的氧化性由弱到强的顺序是 .
(2)实验②中化学反应转移电子的物质的量是 .
(3)写出实验①中发生反应的离子方程式 .
【答案】
(1)SO ![]() 、I2、ClO﹣
、I2、ClO﹣
(2)4mol
(3)ClO﹣+2I﹣+2H+=I2+Cl﹣+H2O
【解析】解:(1)实验①说明氧化性强弱为:ClO﹣>I2 , 实验②说明氧化性强弱为:I2>SO ![]() ,所以在酸性条件下ClO﹣、I2、SO
,所以在酸性条件下ClO﹣、I2、SO ![]() 的氧化性由弱到强的顺序是SO
的氧化性由弱到强的顺序是SO ![]() 、I2、ClO﹣ , 故答案为:SO
、I2、ClO﹣ , 故答案为:SO ![]() 、I2、ClO﹣;(2)实验②说明碘单质把亚硫酸根离子氧化生成硫酸根离子,自身被还原生成碘离子,氧化剂是碘,还原剂是亚硫酸钠,氧化产物是硫酸根离子,所以氧化性强弱为:I2>SO
、I2、ClO﹣;(2)实验②说明碘单质把亚硫酸根离子氧化生成硫酸根离子,自身被还原生成碘离子,氧化剂是碘,还原剂是亚硫酸钠,氧化产物是硫酸根离子,所以氧化性强弱为:I2>SO ![]() ,反应离子方程式为:H2O+I2+SO
,反应离子方程式为:H2O+I2+SO ![]() =SO
=SO ![]() +2I﹣+2H+ , 设转移电子的物质的量为x. H2O+SO
+2I﹣+2H+ , 设转移电子的物质的量为x. H2O+SO ![]() +I2=SO
+I2=SO ![]() +2I﹣+2H+转移电子
+2I﹣+2H+转移电子
1mol 2mol
0.5mol/L×4L x
x= ![]() =4mol,
=4mol,
故答案为:4 mol;(3)实验①说明酸性条件下,次氯酸钠把碘离子氧化生成碘单质,同时自身被还原生成氯离子,该反应中,次氯酸根离子得电子作氧化剂,碘离子失电子是还原剂,氧化产物是碘,所以氧化性强弱为:ClO﹣>I2 , 反应离子方程式为:ClO﹣+2I﹣+2H+=I2+Cl﹣+H2O,故答案为:ClO﹣+2I﹣+2H+=I2+Cl﹣+H2O.
根据同一化学反应中,氧化剂的氧化性大于氧化产物的氧化性判断ClO﹣、I2、SO42﹣的氧化性强弱;实验②说明碘单质把亚硫酸根离子氧化生成硫酸根离子,自身被还原生成碘离子,根据亚硫酸钠和转移电子的关系式计算转移电子的物质的量;实验①说明酸性条件下,次氯酸钠把碘离子氧化生成碘单质,同时自身被还原生成氯离子.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】在室温下,向Cu(IO3)2饱和溶液中加入足量的经稀硫酸酸化的KI溶液,产生碘化亚铜(CuI)沉淀,溶液由蓝色变为棕黄色,反应前加入淀粉溶液不变蓝,反应后加入淀粉溶液变为蓝色.
(1)该反应中氧化剂是;
(2)该反应的氧化产物是;
(3)1mol氧化剂在反应中得到电子的物质的量为;
(4)某反应体系中有物质:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4 . 请将NaBiO3之外的反应物与生成物分别填入以下空格内,配平化学计量数,并用单线桥表示电子转移的方向和数目. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 中和10 mL 0.1molL-1醋酸与中和100 mL 0.01molL-1的醋酸所需同种碱溶液的用量不同
B. 两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1=10c2
C. 常温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D. 向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种无色可溶性盐分别是由Na+、Mg2+、Ag+、Ba2+、Cl﹣、CO ![]() 、HCO
、HCO ![]() 、NO
、NO ![]() 中不同的阴阳离子所组成.A溶液与硫酸反应只有气体生成,B溶液与硫酸反应只有沉淀生成,C溶液与硫酸反应既有气体又有沉淀生成,D溶液与硫酸反应既无气体又无沉淀生成,则
中不同的阴阳离子所组成.A溶液与硫酸反应只有气体生成,B溶液与硫酸反应只有沉淀生成,C溶液与硫酸反应既有气体又有沉淀生成,D溶液与硫酸反应既无气体又无沉淀生成,则
(1)D为;(写化学式)
(2)分别写出下列反映的三个离子方程式①A与足量的硫酸溶液;
②C与足量的硫酸溶液;
③C与少量的氢氧化钠溶液 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂、蛋白质是人类基本营养物质,关于糖类、油脂、蛋白质的说法正确的是( )
A.单糖可以发生水解反应
B.油脂皂化是取代反应,硬化也是取代反应
C.蛋白质水解的最终产物均为氨基酸
D.饱和Na2SO4、CuSO4溶液均可用于蛋白质的盐析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质按纯净物、混合物、强电解质、弱电解质、非电解质的顺序组合正确的是( )
纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
A | 盐酸 | 水煤气 | 硫酸 | 醋酸 | HD |
B | 胆矾 | 石灰水 | 硫酸钡 | HNO2 | NH3 |
C | 火碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
D | 冰醋酸 | 福尔马林 | 苛性钾 | 碘化氢 | 乙醇 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国本土科学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理和医学奖.已知二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( ) 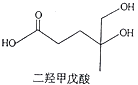
A.与乙醇发生酯化反应生成产物的分子式为C8H18O4
B.能发生加成反应,不能发生取代反应
C.在铜的催化下与氧气反应的产物可以发生银镜反应
D.标准状况下1mol该有机物可以与足量金属钠反应产生22.4L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列短周期元素相关性质的数据:
元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
原子半径(10﹣10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
最低负化合价 | ﹣2 | ﹣3 | ﹣1 | ﹣3 |
试回答下列问题:
(1)元素⑤在周期表中的位置;
(2)元素④与元素⑦相比较,气态氢化物较稳定的是(填结构式);
(3)元素④形成的+3和+5价的氯化物中,各原子均达到8电子稳定结构的化合物是(写化学式);
(4)以下叙述正确的是 .
A.氢化物的沸点为④<⑦
B.①与②形成的化合物具有两性
C.与稀盐酸反应单质②比单质⑥快
D.最高价氧化物对应水化物的碱性③>⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用碳酸钠晶体(Na2CO310H2O)来配制1.0molL﹣1 Na2CO3溶液500mL,假如其他操作均准确无误,下列情况会引起所配溶液浓度偏高的是( )
A.称取碳酸钠晶体53.0g
B.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗
C.定容时,俯视观察刻度线
D.定容后,将容量瓶反复倒转、摇匀、静置时发现液面低于刻度线,于是又加入少量水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com