
�����13�֣����Ĵ������ǹ�ҵ���������Ҫ��Ӧ��500��C���䷴Ӧ����ʽΪ��
4NH3(g) +5O2(g) 4NO(g)+6H2O(g)+Q�����������գ�
4NO(g)+6H2O(g)+Q�����������գ�
23.���Ҫ���������Ӧ�ķ�Ӧ���ʣ����Բ�ȡ�Ĵ�ʩ��
a.��ѹ b.����NH3��Ũ�� c.���� d.��ˮҺ������
24.��500��ʱ����2L�ܱ������м���10mol NH3��10mol O2���������淴Ӧ�ﵽƽ�⣬������ͼ��ʾ����aʱ�̸ı䷴Ӧ���������´ﵽƽ�⣬�øı������������ ���Ƚ�bʱ����cʱ�̷�Ӧ����ת���ʴ�С���>����<����b c�������������䣬cʱ�̼�ѹ����ƽ�������ƶ�����ԭ������� ������dʱ�����´ﵽƽ�⣬����ͼ�л���c��d����ر仯ͼ��

25.��ҵ�����Ϳ���Ϊԭ���������ᣬ�뻭�����Ṥҵ����������ͼ��
26.���е�Ԫ��ԭ�����������Ų��Ĺ������ʽ�� ��������Ԫ��ԭ�����γɵ���N3-�����Ų���ͬ����������Ӧ��ԭ�ӵİ뾶�Ӵ�С������˳��Ϊ �����зǽ���Ԫ���γɵ��⻯����ȶ�����ǿ����Ϊ��˳��Ϊ���û�ѧʽ��ʾ�� ��
27.��֪NH3��N2H4���ǵ����⻯�N2H4�ĵ���ʽ�� ��NH3��N2H4�����л�ԭ�ԣ�����������ǿ��������Ӧ��������һ�������£������Ա�˫��ˮ����Ϊ����̬����д���÷�Ӧ�Ļ�ѧ����ʽ ��
��23��2�֣�25��2�֣�����ÿ��1�֣�23.bc 24. ���»��ѹ��<�����ܼ�ѹ��ˮ��Һ��
 25.
25. 
26.  ��Na>Mg>Al>O>F��HF>H2O>NH3
��Na>Mg>Al>O>F��HF>H2O>NH3
27. 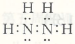 2NH3+3H2O2��N2+ 6H2O
2NH3+3H2O2��N2+ 6H2O
��������
���������23.a.��ѹ��Ӧ���ʼ�С��a����b.����NH3��Ũ�ȷ�Ӧ���ʼӿ죬b��ȷ��c.���·�Ӧ���ʼӿ죬c��ȷ��d.��ˮҺ�����ߣ�����������Ũ�ȣ���Ӧ���ʽ��ͣ�d����ѡbc��
24.��500��ʱ����2L�ܱ������м���10mol NH3��10mol O2���������淴Ӧ�ﵽƽ�⣬������ͼ��ʾ��
����ͼ���֪��aʱ�����淴Ӧ���ʾ�˲�������淴Ӧ���ʴ�������Ӧ����˵��ƽ�����淴Ӧ������С���������Ӧ���������ķ��ȷ�Ӧ����ı�ķ�Ӧ�����������¶Ȼ�����ѹǿ������ͼ����ж�b��c�Ĺ���������Ӧ��������淴Ӧ���ʣ�����Ӧ������Ӧ������У���Ӧ����ת������b��c�������������䣬cʱ�̼�ѹ����ƽ�������ƶ�����˵������Ӧ�����С�������ԭ������ǿ��ܼ�ѹ��ˮ��Һ������������������֪c��d����ر仯ͼ����Ա�ʾΪ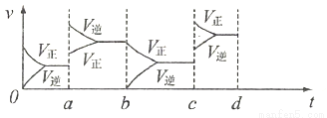 ��
��
25.�������ȷ�������������NO��Ȼ��NO����������NO2��NO2����ˮת��Ϊ���ᣬ�����Ṥҵ����������ͼ�ɱ�ʾΪ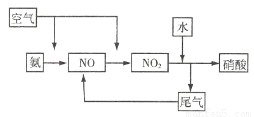 ��
��
26.��Ԫ�ص�ԭ��������7����Ԫ��ԭ�����������Ų��Ĺ������ʽ�� ��ͬ������������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶�������������Ԫ��ԭ�����γɵ���N3-�����Ų���ͬ����������Ӧ��ԭ�ӵİ뾶�Ӵ�С������˳��ΪNa>Mg>Al>O>F���ǽ�����Խǿ���⻯����ȶ���Խǿ�����⻯���ȶ���ǿ��˳����HF>H2O>NH3��
��ͬ������������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶�������������Ԫ��ԭ�����γɵ���N3-�����Ų���ͬ����������Ӧ��ԭ�ӵİ뾶�Ӵ�С������˳��ΪNa>Mg>Al>O>F���ǽ�����Խǿ���⻯����ȶ���Խǿ�����⻯���ȶ���ǿ��˳����HF>H2O>NH3��
27.��֪NH3��N2H4���ǵ����⻯���˿��Կ����ǰ��������е�һ����ԭ�ӱ�����ȡ������N2H4�ĵ���ʽ��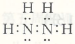 ����һ�������£������Ա�˫��ˮ����Ϊ����̬��������������������ԭ���غ��֪����ˮ���ɣ���÷�Ӧ�Ļ�ѧ����ʽΪ2NH3+3H2O2��N2+ 6H2O��
����һ�������£������Ա�˫��ˮ����Ϊ����̬��������������������ԭ���غ��֪����ˮ���ɣ���÷�Ӧ�Ļ�ѧ����ʽΪ2NH3+3H2O2��N2+ 6H2O��
���㣺������������Է�Ӧ���ʺ�ƽ��״̬��Ӱ���Լ�Ԫ�������ɡ����ʽṹ���й��ж�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ�����и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��8�֣�ijС��Թ������Ƶ����ʺ���;����̽����
��1���۲�����ۣ��ɻ�֪������������ ��
��2����CuSO4��Һ����ʢ������Na2O2������Թ��У����Թ۲쵽�������� ��������Ӧ�Ļ�ѧ����ʽ����Ϊ ��
��3��Na2O2������DZˮͧ����Ϊ��������Դ��������100g Na2O2�������ɱ�״���¶��������O2����д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�����в�ƽ����һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��1 mol H2��ռ���ԼΪ22.4 L
B��22 g CO2�к��еķ�����ԼΪ6.02��1023
C��100 mL 0.5 mol/L NaOH��Һ�к����ʵ�����Ϊ0.05 g
D����״���£�11.2 L O2��H2�Ļ����������������ԼΪ3.01��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�����в�ƽ����һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������һ�����ʵ���Ũ�ȵ���Һʱ�������õ���������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��л�����������ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ��ƶ���
�����14�֣���ŵ����һ�ֽ�����ʹҩ����ø�������¿����ͷų���˾ƥ�ֺ�����Ϣʹ����ṹΪ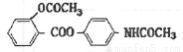 ����ϳ�;�����£�
����ϳ�;�����£�

���������գ�
45.��Ӧ�ٵķ�Ӧ����Ϊ ���л���A������Ϣʹ��ʽ�����
46.��ŵ�������ĺ�����������
47.д����Ӧ�ڵĻ�ѧ����ʽ ��
48.���ڰ�˾ƥ������������ȷ���ǣ���ѡ���ţ�
A.�����Ȼ�����Һ������ɫ��Ӧ B.����������ͭ����Һ��Ӧ
C.�ܷ�����ȥ��Ӧ D.�ܷ���������Ӧ
49.������������������Ϣʹ��ͬϵ�ﹲ�� �֣�д������һ�ֵĽṹ��ʽ ��
��̼ԭ����������Ϣʹ��2�� �ڱ�����ֻ��2����λ��֧�� �ۺ���2����
50.����֪

���Ա��Ӻ��������� ��Ϊ�л�ԭ�ϣ��ϳɰ�˾ƥ�֣������������кϳ�;�����ϳ�·�߳��õı�ʾ����Ϊ��
��Ϊ�л�ԭ�ϣ��ϳɰ�˾ƥ�֣������������кϳ�;�����ϳ�·�߳��õı�ʾ����Ϊ�� ����
����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��л�����������ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�������ȷ���ܴﵽԤ��Ŀ�ĵ���
ʵ��Ŀ�� | ���� | |
A | ֤����������Ư���� | ����������ͨ����ˮ����ˮ��ɫ |
B | ֤��̼������ǿ�ڱ��� | �ڱ�������Һ��ͨ�������̼����Һ����� |
C | ��ȥ���л��еı����� | ��������������Һ�����÷�Һ |
D | �Ƚ�пͭ���������� | �õ�����������ʯī�缫������ZnSO4��CuSO4 �Ļ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��л�����������ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ij������Һ�����ܺ���Br-��SO42-��HSO3-��NH4+)���ֱ��������ʵ�飺�ټ���ʱ�ų��������ʹƷ����Һ��ɫ���ڼ������Һʹ��Һ�ʼ��ԣ��ټ���ʱ�ų��������ʹʪ��ĺ�ɫʯ����ֽ�������ۼ�����ˮʱ����Һ�ԳʳȺ�ɫ���ܼ���BaCl2Һ��ϡ���ᣬ����������ϡ����İ�ɫ��������������������ȷ������ԭ��Һ���Ƿ���ڵ���
A��Br- B��SO42- C��HSO3- D��NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������и߸����ڶ����¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й����Ȼ�ѧ��Ӧ����������ȷ����
A����֪H��(aq)��OH��(aq)== H2O(l) ��H����57.3 kJ��mol��1����H2SO4��Ba(OH)2��Ӧ�ķ�Ӧ�Ȧ�H��2��(��57.3) kJ��mol��1
B�������ǵ�ȼ������2800 kJ��mol��1����1/2C6H12O6(s)��3O2(g)==3CO2(g)��3H2O(l) ��H��1400 kJ/mol
C��H2(g)��ȼ������285.8 kJ��mol��1����2H2O(g)==2H2(g)��O2(g) ��H��+571.6 kJ��mol��1
D��ȼ�ϵ���н��״�����ת��Ϊ�������Ȼ�ѧ����ʽ�ǣ�CH3OH(g)��1/2O2(g)== CO2(g)��2H2(g)��H����192.9 kJ��mol��1��CH3OH(g)��ȼ����Ϊ192.9 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��о�����������ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��a gC2H4��C3H6�Ļ���ﺬ��b��C-H�������ӵ��������Ա�ʾΪ
A��7a/b B��7b/a C��14a/b D��b/14a
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com