
【题目】实验室需要配制0.50 mol·L—1 NaCl溶液480 mL。按下列操作步骤填上适当的文字,使整个操作完整。
(1)选择仪器。完成本实验必须用到的仪器有:托盘天平(带砝码,最小砝码为5g)、量筒、药匙、烧杯、玻璃棒、____________、____________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体____________g。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:
![]()
②称量过程中NaCl品体应放于天平的____________(填“左盘”或“右盘”)。
③称量完毕,将药品倒人烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是________________________。
(5)移液、洗涤。在移液时应使用________________________引流,需要洗涤烧杯2~3次是为了____________________________________。
(6)定容。向容量瓶中加水至液面接近刻度线____________处,改用____________加水,使溶液凹液面与刻度线相切。
(7)摇匀、装瓶。
【答案】 500 mL容量瓶 胶头滴管 14.6 ![]() 左盘 搅拌,加速NaCl溶解 玻璃棒,保证溶质全部转入容量瓶中 1~2 cm 胶头滴管
左盘 搅拌,加速NaCl溶解 玻璃棒,保证溶质全部转入容量瓶中 1~2 cm 胶头滴管
【解析】
(1)配制一定物质的量浓度溶液的一般步骤,用到的仪器有:托盘天平(精确到0.1g)、药匙、等质量的两片滤纸、烧杯、玻璃棒、500mL容量瓶、胶头滴管,因此还缺少500mL容量瓶、胶头滴管;
(2)要配制0.50mol/L NaCl溶液480mL,需要500mL容量瓶,需要氢氧化钠的质量m=0.5L×0.50mol/L×58.5g/mol=14.6g;
(3)①由于最小砝码为5g,则称量时砝码质量为10g,游码的质量为4.6g,因此游码应该为![]() ;
;
②用托盘天平称量物质应遵循左物右码原则,所以称量过程中NaCl晶体应放于天平的左盘;
(4)溶解的实验中需要使用玻璃棒进行搅拌,加速氯化钠的溶解;
(5)转移溶液时需要使用玻璃棒引流,避免溶液流到容量瓶以外;定容前还应该洗涤烧杯和玻璃棒,目的是将溶质全部转移到容量瓶中;
(6)定容时向容量瓶中加水至液面接近刻度线1~2 cm处,改用胶头滴管加水,使溶液凹液面与刻度线相切。


科目:高中化学 来源: 题型:
【题目】利用熔融碱焙烧工艺可从铝热法生产金属铬的铬渣(Al、Al2O3、Cr2O3等)中浸出铬和铝,为实现铬和铝的再生利用。其工作流程如下:

(1)铝热法冶炼金属铬,是利用了金属铝的__________(填“氧化性”或“还原性”)。
(2)溶液1中的阴离子有CrO42-、__________。
(3)过程I,在Cr2O3参与的反应中,若生成0.4molCrO42-,消耗氧化剂的物质的量是__________。
(4)通入CO2调节溶液pH实现物质的分离。
①滤渣A煅烧得到Al2O3,再用电解法冶炼Al。冶炼Al的化学方程式是____________________。
②滤渣B受热分解所得物质的循环利用,B是__________。
③已知:2CrO42-+2H+![]() Cr2O72-+H2O K=4.0×1014
Cr2O72-+H2O K=4.0×1014
滤液3中Cr2O72-的溶度是0.04mol/L,则CrO42-的浓度是__________mol/L。
(5)过程II的目的是得到K2Cr2O7粗品。不同温度下化合物的溶解度(g/100gH2O)
化合物名称 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 |
K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 |
K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 |
Na2Cr2O7 | 163 | 183 | 215 | 269 | 376 |
结合表中数据分析,过程II的操作是:____________________,过滤,得到K2Cr2O7粗品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向体积为2 L的恒容密闭容器中加入足量铁粉和0.08 mol H2O(g),发生反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g),一段时间后达平衡。t1时刻向容器中再充入一定量的H2,再次达平衡时H2的体积分数为20%。下列说法正确的是( )
Fe3O4(s)+4H2(g),一段时间后达平衡。t1时刻向容器中再充入一定量的H2,再次达平衡时H2的体积分数为20%。下列说法正确的是( )
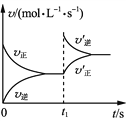
A. t1时刻充入H2,v′正、v′逆变化如右图
B. 第一次达平衡时,H2的体积分数小于20%
C. 温度为T时,起始向原容器中充入0.1 mol铁粉、0.04 mol H2O(g)、0.1 mol Fe3O4(s)、0.005 mol H2(g),反应向正反应方向进行
D. 温度为T时,向恒压容器中加入足量Fe3O4(s)和0.08 mol H2 (g),达平衡时H2(g)转化率为20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑灰的主要成分是硫化钡(BaS),常用于制取氧化钡等钡盐。
I.工业上常用如下方案测定黑灰中BaS含量:
步骤:准确称取一定质量黑灰试样置于烧杯中,加入适量的蒸馏水使黑灰充分溶解。
步骤2:过滤并洗涤残留固体2~3次,将滤液、洗涤液合并后完全转移至500mL容量瓶中,加水定容。
步骤3:取20.00mL步骤2中溶液于锥形瓶中,再迅速加入10mL2%醋酸稀溶液及25.00mL 0.5mo1/L碘标准溶液(过量),充分振荡,使BaS完全转化为S。
步骤4向锥形瓶中加入2-3滴淀粉溶液,用0.1mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液体积VmL(I2+2S2O32-=2I-+S4O62-)。
步骤5....
步骤6数据处理,计算黑灰中BaS含量。
(1)步骤2实验中所需的玻璃仪器有烧杯、漏斗.500mL容量瓶、_______。
(2)步骤4到达滴定终点时,滴定管中液面如图所示,此时滴定管读数为____mL。若盛装Na2S2O3标准溶液的滴定管未润洗,则所测得的BaS含量将会_______(填“偏高”、“偏低"或“不变”)。

(3)为保证实验结果的准确性,步骤5应为_______________。
II.氯化钡可用于测定煤矿酸性矿井水中硫酸盐的含量。
(1)酸性矿井水(主要含有H+、Fe2+、SO42-)是煤层中夹杂的硫铁矿(FeS2)被空气中氧气氧化所致,该反应的离子方程式为_______________。
(2)查阅资料发现铁元素的存在对SO2含量(mg/L)的测定结果影响较大。请补充完整测定酸性矿井水中SO42-含量的实验步骤:量取一定体积的酸性矿井水,________,根据采集的数据计算废水中SO42-含量。
(实验中须使用的试剂有:稀氨水、30%双氧水、1mol/LBaCl2溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO和O2经反应①和反应②转化为NO2,其能量变化随反应进程的图示如下。

①2NO(g)![]() N2O2(g)△H1平衡常数K1
N2O2(g)△H1平衡常数K1
②N2O2(g)+O2(g)![]() 2NO2(B)△H2平衡常数K2
2NO2(B)△H2平衡常数K2
下列说法不正确的是( )
A. △H1<0,△H2<0
B. 2NO(g)+O2(g)![]() 2NO2(g)的平衡常数K=K1/K2
2NO2(g)的平衡常数K=K1/K2
C. 表示2NO(g)+O2(g)![]() 2NO2(g)的△H=△H1+△H2
2NO2(g)的△H=△H1+△H2
D. 反应②的速率大小决定2NO(g)+O2(g)![]() 2NO2(g)的反应速率
2NO2(g)的反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B. 25℃时,等体积等物质的量浓度的硝酸与氨水混合后,溶液pH=7
C. 25℃时,0.1mol/L的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱
D. 25℃时,pH=2的酸HA溶液与pH=12的玻BOH溶液等体积混合后,所得溶液呈酸性,证明HA为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金是一类用途广泛的金属材料,下列关于合金的描述正确的是( )
A.合金的硬度比组成它的成分金属小
B.在我国,使用最早的合金是青铜
C.合金的熔点一般比组成它的成分金属高
D.目前用量最大、用途最广的合金是铝合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,正确的是( )
A.H2SO4=H2++SO42﹣
B.Ba(OH)2=Ba2++OH ﹣
C.NaNO3=Na ++NO3﹣
D.CuSO4=Cu+2+SO4﹣2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com