
【题目】乙烯是重要的有机化工初始原料,可以由它出发合成很多有机产品,油漆软化剂丁烯酸乙酯的合成途径如下:

完成下列填空:
(1)丁烯酸乙酯的结构简式为______________________________。
(2)C→D的反应类型是____________。
A→B的化学方程式为___________________________________。
(3)写出一种D的同分异构体(与D含有完全相同的官能团)。_________________________________________
(4)请设计实验,检验D是否完全氧化为丁烯酸。____________________________
(5)设计一条由C制备ClCH2CH=CHCH2Cl的合成路线。(合成路线常用的表示方式为:A ![]() B
B ![]() 目标产物)_____________
目标产物)_____________
【答案】 CH3CH=CHCOOC2H5 消去反应 2C2H5OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O ![]() 或CH2=CHCH2CHO 取样,加入过量氢氧化钠溶液,然后加入新制氢氧化铜,加热煮沸,若出现砖红色沉淀,则D没有完全氧化;若不出现砖红色沉淀,则D完全氧化了
或CH2=CHCH2CHO 取样,加入过量氢氧化钠溶液,然后加入新制氢氧化铜,加热煮沸,若出现砖红色沉淀,则D没有完全氧化;若不出现砖红色沉淀,则D完全氧化了 ![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】(1)乙烯与水加成生成A是乙醇,乙醇催化氧化生成B是乙醛,两分子乙醛加成生成C,C发生消去反应生成D,D氧化生成丁烯酸,丁烯酸与乙醇酯化生成丁烯酸乙酯,则丁烯酸乙酯的结构简式为CH3CH=CHCOOC2H5。(2)C→D的反应类型是消去反应。A→B的化学方程式为2C2H5OH+O2![]() 2CH3CHO+2H2O。(3)与D含有完全相同的官能团有机物结构简式为CH2=C(CH3)CHO或CH2=CHCH2CHO。(4)检验D是否完全氧化为丁烯酸可以通过检验醛基,即取样,加入过量氢氧化钠溶液,然后加入新制氢氧化铜,加热煮沸,若出现砖红色沉淀,则D没有完全氧化;若不出现砖红色沉淀,则D完全氧化了。(5)根据逆推法结合C的结构简式可知制备ClCH2CH=CHCH2Cl的合成路线为
2CH3CHO+2H2O。(3)与D含有完全相同的官能团有机物结构简式为CH2=C(CH3)CHO或CH2=CHCH2CHO。(4)检验D是否完全氧化为丁烯酸可以通过检验醛基,即取样,加入过量氢氧化钠溶液,然后加入新制氢氧化铜,加热煮沸,若出现砖红色沉淀,则D没有完全氧化;若不出现砖红色沉淀,则D完全氧化了。(5)根据逆推法结合C的结构简式可知制备ClCH2CH=CHCH2Cl的合成路线为![]()
![]()
![]()
![]()
![]()
![]()
![]() 。
。


科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( ) 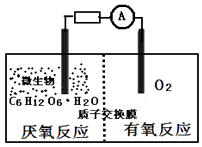
A.负极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从正极区移向负极区
D.电池总反应为C6H12O6+6O2═6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性碳催化下合成.
(1)实验室中常用来制备氯气的化学方程式为;
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为﹣890.3kJmol﹣1、﹣285.8 kJmol﹣1和﹣283.0 kJmol﹣1 , 则生成1 m3(标准状况)CO所需热量为;
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为;
(4)COCl2的分解反应为COCl2(g)═Cl2(g)+CO(g)△H=+108 kJmol﹣1 . 反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出): 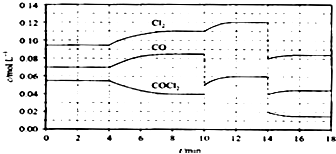
①计算反应在第8min时的平衡常数K=;
②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2) T(8)(填“<”、“>”或“=”);
③若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)=molL﹣1
④比较产物CO在2﹣3min、5﹣6min和12﹣13min时平均反应速率[平均反应速率分别以v(2﹣3)、v(5﹣6)、v(12﹣13)表示]的大小;
⑤比较反应物COCl2在5﹣6min和15﹣16min时平均反应速率的大小:v(5﹣6) v(15﹣16)(填“<”、“>”或“=”),原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式不正确的是( )
A. 硫酸型酸雨的形成会涉及反应:2H2SO3+O2===4H++2SO![]()
B. 热的纯碱溶液可以清洗油污的原因:CO![]() +2H2O
+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
C. 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-===SiO![]() +H2O
+H2O
D. 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+===Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与醋酸有关的反应方程式正确的是
A. 与烧碱反应:OH-+CH3COOH → CH3COO-+H2O
B. 与CaCO3反应:CO32-+2CH3COOH → 2CH3COO-+CO2↑+H2O
C. 乙醛氧化:CH3CHO+O2 ![]() CH3COOH
CH3COOH
D. 制乙酸乙酯:CH3COOH+C2H518OH ![]() CH3COOC2H5+H218O
CH3COOC2H5+H218O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,无水硫酸铜粉末受热分解生成CuO和气体A。气体A为SO2、SO3和O2中的一种或几种。请回答:
(1)气体A的合理组成为如下三种情况:
①只有SO3 ②_________ ③三种气体都有
(2)只用一种试剂就能证明气体A中是否含有SO2,该试剂是_______________。
A.石蕊试液 B.品红溶液 C. BaCl2溶液 D. NaOH溶液
(3)若气体A中SO2、SO3和O2都有,用下图所示装置测定其中O2的体积。测定结果比实际值明显偏低,其原因是________________。
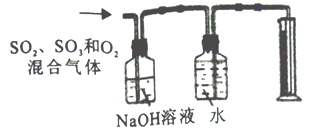
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 用惰性电极电解CuSO4溶液![]()
B. 在Na2SiO3溶液中加入盐酸:![]()
C. 在稀硝酸中加入过量的铁屑![]()
D. 在NaHCO3溶液中加入过量Ba(OH)2溶液![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
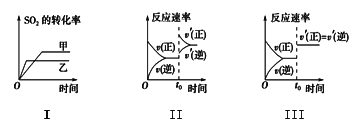
A. 图Ⅰ研究的是温度对此化学平衡的影响,且乙的温度较高
B. 图Ⅱ研究的是t0时刻增大体系的压强对反应速率的影响
C. 图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响
D. 图Ⅲ研究的是t0时刻使用催化剂对化学平衡的影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com