
(选考)【化学——物质结构与性质】(15分)
W、Q、R、X、Y、Z六种元素的原子序数逐渐增大。已知W原子1s轨道上只有一个电子,Q、X原子p轨道的电子数分别为2和4,Z的原子序数为29,除Z外均为短周期主族元素,Y原子的价电子排布为(n+1)sn(n+1)pn。请回答下列问题:
(1)Q和W能形成一种化合物的相对分子质量为28,则该化合物的中心原子采取的杂化轨道类型是 ,该分子中含有____个 键。
键。
(2)Z原子的核外电子排布式为 ;向Z的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体中Z的离子与NH3之间的化学键为 。
(3)这六种元素中,电负性最大与最小的两种非金属元素形成的晶体属于____晶体;W、Q、X三种元素之间可以形成多种化合物,其中邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,理由是 。邻甲基苯甲醛分子中碳原子轨道的杂化类型为 。1 mol 苯甲醛分子中σ键为 mol。
(4)元素X的阴离子Xn-中所有电子正好充满K和L电子层,CnX晶体的最小结构单元如图所示。

该晶体中阳离子和阴离子个数比为____,晶体中每个Xn-被 个等距离的C+离子包围。
(1)sp2杂化(1分)1(1分) (2)[Ar]3d104s1;(或1s22s22p63s23p63d104s1)(1分)
配位键(1分) (3)原子(1分)邻羟基苯甲醛形成分子内氢键,对羟基苯甲醛能在分子间形成氢键(2分) sp2 和sp3 (2分) 14(2分)(4)3:1(2分) 6(2分)
【解析】
试题分析:W、Q、R、X、Y、Z六种元素的原子序数逐渐增大。已知W原子1s轨道上只有一个电子则W是H。Q、X原子p轨道的电子数分别为2和4,这说明Q是C,X是O,则R是N。Z的原子序数为29,则Z是Cu。除Z外均为短周期主族元素,Y原子的价电子排布为(n+1)sn(n+1)pn,则n=2,所以Y是Si元素。
(1)Q和W能形成一种化合物的相对分子质量为28,该化合物是乙烯。乙烯是平面型结构,则该化合物的中心原子采取的杂化轨道类型是sp2杂化。单键都是σ键,而双键是由1个σ键和1个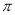 键构成,则根据乙烯的结构简式CH2=CH2可知该分子中含有1个
键构成,则根据乙烯的结构简式CH2=CH2可知该分子中含有1个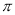 键。
键。
(2)铜的原子序数是29,根据核外电子排布规律可知,原子的核外电子排布式为[Ar]3d104s1(或1s22s22p63s23p63d104s1);向Z的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体是配合物,其中铜离子与NH3之间的化学键为配位键。
(3)同主族自上而下电负性逐渐减小,同周期自左向右电负性逐渐增大,则这六种元素中,电负性最大是氧元素,最小的非金属是硅元素,两种非金属元素形成的晶体是二氧化硅,属于原子晶体;由于邻羟基苯甲醛形成分子内氢键,对羟基苯甲醛能在分子间形成氢键,分子间氢键强于分子内氢键,所以邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点;甲基碳原子是饱和碳原子,属于sp3杂化。醛基和苯环上的碳原子是sp2杂化,则邻甲基苯甲醛分子中碳原子的杂化类型为sp2 和sp3。单键都是σ键,而双键是由1个σ键和1个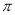 键构成,则根据苯甲醛的结构简式
键构成,则根据苯甲醛的结构简式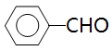 可知1 mol 苯甲醛分子中σ键为14mol。
可知1 mol 苯甲醛分子中σ键为14mol。
(4)根据晶胞结构可知X原子的个数=8×1/8=1,C原子数=12×1/4=3,所以该晶体中阳离子和阴离子个数比为3:1。晶体中每个Xn-被6个等距离的C+离子包围,即上下左右前后各1个。。
考点:考查物质结构与性质模块的分析与判断


科目:高中化学 来源:2014-2015甘肃省白银市高二上学期期末化学试卷(解析版) 题型:选择题
下列物质中,属于弱电解质的是
A.CO2 B.NH3·H2O C.NH4NO3 D.C2H5OH(酒精)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邯郸市高三上学期1月教学质量检测化学试卷(解析版) 题型:选择题
下列实验装置进行的相应实验,能达到实验目的的是

A.装置甲可用于检验有乙烯生成
B.装置乙可用于收集和吸收氨气
C.装置丙可用于除去Cl2中混有的HCl气体
D.装置丁可分离CH3COOC2H5和饱和碳酸钠溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邯郸市高三上学期1月教学质量检测化学试卷(解析版) 题型:选择题
NA为阿伏伽德罗常数的数值,下列叙述错误的是
A.标准状况下,11.2 L氦气中含有0.5 NA原子
B.标准状况下,0.1 mol Cl2参加反应,转移的电子数目一定为0. 2 NA
C.常温常压下,46g NO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移电子总数NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三上学期期末理综化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式的是
A.NO2与水的反应:3NO2+H2O=2NO3-+NO+2H+
B.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
C.向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+=SO2↑+H2O
D.NH4HCO3溶于过量的NaOH溶液中:HCO3-+ OH-=CO32-+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三上学期期末化学试卷(解析版) 题型:实验题
(10分)Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如下。

已知:I.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
II.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是_____________。
(2)吸收塔中的原料B可以选用____________(填字母序号)。
a.NaCl溶液 b.Na2CO3溶液 c.Na2SO4溶液
(3)某小组同学用下图装置模拟制备Na2S2O3的过程(加热装置已略去)。

①A中使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是______。装置B的作用是_______。
②C中制备Na2S2O3发生的连续反应有:Na2S +H2O +SO2===Na2SO3 +H2S、_____和__________。
(4)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为_________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三上学期期末化学试卷(解析版) 题型:选择题
下列与金属腐蚀有关的说法中,不正确的是
A.钢铁在潮湿空气中生锈属于电化学腐蚀
B.电化学腐蚀一般可分为吸氧腐蚀和析氢腐蚀
C.金属腐蚀的本质是金属原子失去电子被氧化的过程
D.铝具有很强的抗腐蚀能力,是因为其不易与氧气发生反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省部分高三1月份统一考试理综化学试卷(解析版) 题型:选择题
【化学一物质结构与性质】(15分)
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素n的基态原子的价电子排布式 ,元素O在周期表的位置是 ,属于 区。
(2)k在空气中燃烧产物的分子构型为 ,中心原子的杂化方式为 ,该分子是 (填“极性”或“非极性”)分子。
(3)第三周期8种元素按单质熔点高低的顺序如左下图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填下图中的序号)。

(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如右下图乙所示。则晶胞中i原子的配位数为 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com