
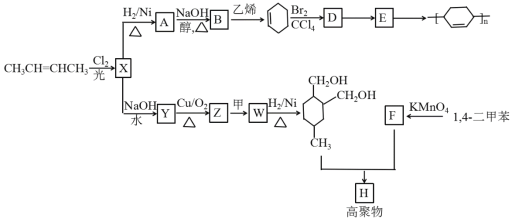
����Ŀ����ϩ��Ϊԭ�ϣ��ϳ�ijЩ�߾����·�����£�
��֪����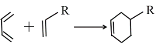 ��R����ȡ�������⣩��
��R����ȡ�������⣩��
��Ϊ������F����NaHCO3��Ӧ����CO2��������������⣺
��1��CH3CH=CHCH3��������_________��X�й����ŵ�������______________��
��2��A��B�Ļ�ѧ����ʽ��________________________________________��
��3��D��E�ķ�Ӧ����Ϊ��______��
��4�������й�˵����ȷ����_________��
a.�л���Y��HOCH2CH2OH��Ϊͬϵ��
b.�л���Z�ܷ���������Ӧ
c.�л���Y�ķе��B��
d.�л���F���뼺�������۳ɾۺ���
��5��д��Z��W�Ļ�ѧ����ʽ��____________________��
��6��Y��ͬ���칹���У�������������______�֡�
��7���߾���H�Ľṹ��ʽ��_______________��
���𰸡�2-��ϩ ̼̼˫������ԭ�� ClCH2CH2CH2CH2Cl +2NaOH![]() CH2=CH��CH=CH2+ 2NaCl+2H2O ��ȥ��Ӧ b d
CH2=CH��CH=CH2+ 2NaCl+2H2O ��ȥ��Ӧ b d ![]() 4
4 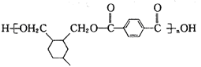
��������
2-��ϩ����������ȡ����Ӧ����X��X�����������ӳɷ�Ӧ����A��A���������ƵĴ���Һ������ȥ��Ӧ����B��B���Ҵ���Ӧ���ɻ���ϩ����������Ϣ֪��B��1��3-����ϩ��A��1��4-���ȶ��飬X��1��4-����-2-��ϩ������ϩ���巢���ӳɷ�Ӧ����DΪ1��2-���廷���飬1��2-���廷���鷢����ȥ��Ӧ����E��E�����Ӿ۷�Ӧ����![]() ��1��4-����-2-��ϩ���������Ƶ�ˮ��Һ����ȡ����Ӧ����Y Ϊ1��4-���ǻ�-2-��ϩ��1��4-���ǻ�-2-��ϩ��������������Z��Z�Ľṹ��ʽΪ��HOCCH=CHCHO��Z�ͼ�Ӧ����W��W�����������ӳɷ�Ӧ����
��1��4-����-2-��ϩ���������Ƶ�ˮ��Һ����ȡ����Ӧ����Y Ϊ1��4-���ǻ�-2-��ϩ��1��4-���ǻ�-2-��ϩ��������������Z��Z�Ľṹ��ʽΪ��HOCCH=CHCHO��Z�ͼ�Ӧ����W��W�����������ӳɷ�Ӧ����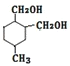 ����������Ϣ֪��Z�ͼ����ӳɷ�Ӧ����W�����ԼĽṹ��ʽΪ��
����������Ϣ֪��Z�ͼ����ӳɷ�Ӧ����W�����ԼĽṹ��ʽΪ��![]() ����Z�����ӳɷ�Ӧ����W��W�Ľṹ��ʽΪ��
����Z�����ӳɷ�Ӧ����W��W�Ľṹ��ʽΪ��![]() ��1��4-���ױ������Ը��������������FΪ1��4-�������ᣬ1��4-���������
��1��4-���ױ������Ը��������������FΪ1��4-�������ᣬ1��4-��������� ����������Ӧ����H����H�Ľṹ��ʽΪ��
����������Ӧ����H����H�Ľṹ��ʽΪ�� ��
��
��1��CH3CH=CHCH3��������2-��ϩ��X��1��4-����-2-��ϩ������X���еĹ�������̼̼˫������ԭ�ӣ�
��2��1��4-���ȶ�����������ƵĴ���Һ������ȥ��Ӧ����1��3-����ϩ����Ӧ����ʽΪ�� ClCH2CH2CH2CH2Cl +2NaOH![]() CH2=CH��CH=CH2+ 2NaCl+2H2O ��
CH2=CH��CH=CH2+ 2NaCl+2H2O ��
��3��1��2-���廷���鷢����ȥ��Ӧ����E��
��4��a���л���Y��1��4-���ǻ�-2-��ϩ��Y�к���̼̼˫����HOCH2CH2OH�в���̼̼˫�������Զ��߲���ͬϵ��ʴ���
b���л���Z�Ľṹ��ʽΪ��HOCCH=CHCHO�������ܷ���������Ӧ������ȷ��
c���л���Y��1��4-���ǻ�-2-��ϩ��B��1��3-����ϩ��Y����Է���������B������Y�ķе��B�ߣ��ʴ���
d���л���F��1��4-�������ᣬ�������뼺�������۳ɾۺ������ȷ��
��ѡbd��
��5���ڴ��������£�Z�����ӳɷ�Ӧ����W����Ӧ����ʽΪ��![]() ��
��
��6��Y��1��4-���ǻ�-2-��ϩ��Y��ͬ���칹���ж��֣����ӽṹ�к�������������ͬ���칹��Ľṹ��ʽΪ��HCOOCH2CH2CH3��HCOOCH��CH3��2��CH3COOCH2CH3��CH3CH2COOCH3����4�֣�
��7��ͨ�����Ϸ���֪��H�Ľṹ��ʽΪ�� ��
��


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ����״��ͱ�����Ļ�ѧԭ����
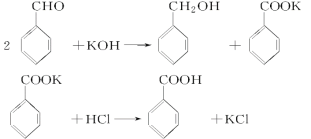
��֪����ȩ�ױ��������������״��ķе�Ϊ205.3 �棻��������۵�Ϊ121.7 �棬�е�Ϊ249 �棬�ܽ��Ϊ0.34 g�����ѵķе�Ϊ34.8 �棬������ˮ���Ʊ����״��ͱ��������Ҫ����������ʾ��
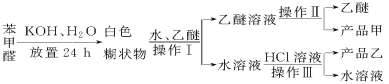
�Ը���������Ϣ�ش��������⣺
��1���������������________��������Һ�����ܽ����Ҫ�ɷ���________��
��2���������������________����Ʒ����________��
��3���������������________����Ʒ����________��
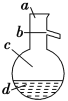
��4����ͼ��ʾ�����������¶ȼ�ˮ�������ط��õ�λ��Ӧ��________(����a����b����c������d��)���ò����У�����������ƿ���¶ȼ��⣬����Ҫ�IJ���������__________________���ռ���Ʒ�������¶�Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��ѧ��Ӧ��ƽ�ⳣ������ʽΪK��![]() ���ڲ�ͬ���¶��¸÷�Ӧ��ƽ�ⳣ�������ʾ�������й���������ȷ����( )
���ڲ�ͬ���¶��¸÷�Ӧ��ƽ�ⳣ�������ʾ�������й���������ȷ����( )
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
A. �÷�Ӧ�Ļ�ѧ����ʽ��CO(g)��H2O(g)![]() CO2(g)��H2(g)
CO2(g)��H2(g)
B. ������Ӧ������Ӧ�Ƿ��ȷ�Ӧ
C. ����1 L���ܱ�������ͨ��CO2��H2��1 mol,5 min���¶����ߵ�830 �棬��ʱ���COΪ0.4 mol����÷�Ӧ�ﵽƽ��״̬
D. ��ƽ��Ũ�ȷ������й�ϵʽ��![]() ��
��![]() �����ʱ���¶�Ϊ1 000 ��
�����ʱ���¶�Ϊ1 000 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȸʯ��Ҫ��Cu2(OH)2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuSO4��5H2O��CaCO3���������£�
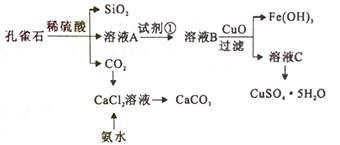
����˵����ȷ����
A. Ϊ����ҺA�е�Fe2+����ΪFe3+���Լ��ٿ�ѡ��˫��ˮ��������
B. ���������ӵ�CuO������Cu����
C. ����ҺC���CuSO4��5H2O����Ҫ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵȲ���
D. �Ʊ�CaCO3ʱ��Ӧ��CaCl2��Һ����ͨ��CO2���ټ��백ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
����ε���Ҫ����Ϊ�������Ρ������(KIO3)�������軯��[K4Fe(CN)6��3H2O]�����������軯�ص���ˮ���ڸ����»ᷢ���ֽ⣺3K4[Fe(CN)6]![]() 2(CN)2��+12KCN+N2��+Fe3C+C
2(CN)2��+12KCN+N2��+Fe3C+C
��ش��������⣺
��1����Fe2+��̬��������Ų�ʽΪ_____��
��![]() �Ŀռ乹��Ϊ______����������������
�Ŀռ乹��Ϊ______����������������
�ۣ�CN��2������̼ԭ���ӻ��������Ϊ_______��һ����CN-��Ϊ�ȵ�����ķ��ӵĵ���ʽΪ_______��
��1molFe(CN)63�к�����������ĿΪ____mol��
��2�������Fe(CO)x������ԭ�Ӽ۵������������ṩ������֮��Ϊ18����x��___��Fe(CO)x�����³�Һ̬���۵�Ϊ��20.5�棬�е�Ϊ103�棬�����ڷǼ����ܼ����ݴ˿��ж�Fe(CO)x��������____(�������)��
��3����ͼ�Ǵ����������Ӿ���Fe3O4��ȡ�����������侧��ṹ��һ�������壬����������Dz���Fe3O4�ľ���______(����������������)�������������������Ӵ���������Χ�ɵ�________(��ռ�ṹ)��϶��
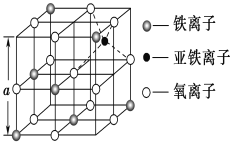
��4��Fe���γɶ������������FeO�����ṹΪNaCl�͡�������ʵ���ϴ��ڿ�λ����λ������ԭ�ӵ�ȱ�ݣ�����ȱ�ݶԾ�������ʻ�����ش�Ӱ�졣���ھ���ȱ�ݣ��ھ�����Fe��O�ĸ����ȷ����˱仯����ΪFexO��x��1���������ijFexO�����ܶ�Ϊ5.71gcm��3�������߳�Ϊ4.28��10��10 m����FexO��x=____�����ô���ʽ��ʾ����Ҫ���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������У�һ����ͬϵ����ǣ� ��
A. C3H8��2-��1-��ϩ
B. 3-��-1-��Ȳ��3-��-1-��Ȳ
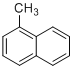
C. ![]() ��
��
D. C4H10��C9H18
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijNa2CO3��NaAlO2�Ļ����Һ����μ���1mol/L�����ᣬ�����Һ�е�CO32-��HCO3-��AlO2-��Al3+�����ʵ��������������Һ������仯��ϵ��ͼ��ʾ��������˵����ȷ����
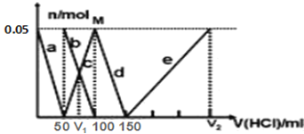
A. a���߱�ʾ�����ӷ���ʽΪ��AlO2-+4H+=Al3++2H2O
B. M��ʱ���ɵ�CO2Ϊ0.05mol
C. ԭ�����Һ�е�CO32-��AlO2-�����ʵ���֮��Ϊ1��2
D. V1��V2=1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 2L �� NaCl��MgCl2��CaCl2 ��ɵĻ��Һ�У���������Ũ�ȴ�С��ͼ��ʾ�������Һ��Ca2�����ӵ����ʵ�����

A. 3.0molB. 2.0molC. 1.0molD. 0.5 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������ԭ��Ӧ���ǣ�������
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com