
乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2与水反应生成乙炔的反应方程式为________.
(2)比较第二周期元素C、N、O三种元素的第一电离能从大到小顺序为 ______(用元素符号表示),用原子结构观点加以解释______。
(3)CaC中C22-与O22+互为等电子体,O22+的电子式可表示为______;1molO22+中含有的Π键数目为_______。
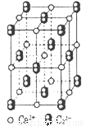
(4)CaC2晶体的晶胞结构与NaCI晶体的相似(如图所示),但CaC2晶体中含有的中哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C22-数目为______。
(5)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为 _______。
(6)乙炔与氢氰酸反应可得丙烯腈(H2C

 =CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是______;分子中处于同一直线上的原子数目最多为______。
=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是______;分子中处于同一直线上的原子数目最多为______。
(1)CaC2+2H2O===CH≡CH↑+Ca(OH)2(2) N>O>C C、N、O原子半径依次减小,原子核对外层电子的吸引力依次增强,元素的第一电离能依次增大;但O原子最外层电子排布为2s22p4,而N原子最外层电子排布为2s22p3,p电子排布处于半充满状态,根据洪特规则特例可知,半充满状态更稳定,所以N元素的第一电离能比O大。(3)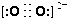 2NA (4)4 (5)1s22s22p63s23p63d10
(6)sp杂化 sp2杂化 3
2NA (4)4 (5)1s22s22p63s23p63d10
(6)sp杂化 sp2杂化 3
【解析】
试题分析:(1) CaC2与水反应生成乙炔的反应方程式为CaC2+2H2O===CH≡CH↑+Ca(OH)2。(2)第二周期元素C、N、O三种元素的第一电离能从大到小顺序为N>O>C,原因是C、N、O三种元素的原子半径依次减小,原子核对外层电子的吸引力依次增强,元素的第一电离能依次增大;但O原子最外层电子排布为2s22p4,而N原子最外层电子排布为2s22p3,p电子排布处于半充满状态,根据洪特规则特例可知,半充满状态更稳定,所以N元素的第一电离能比O大。(3)O22+的电子式可表示为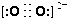 。由O22+的电子式可知在每个O22+中含有2个Π,在1molO22+中含有的Π键数目为2NA。(4)由CaC2晶体的晶胞结构可看出在CaC2晶体中1个Ca2+周围距离最近的C22-数目为4个。(5)Cu是29号元素,其Cu+基态核外电子排布式为1s22s22p63s23p63d10
。 (6)在丙烯腈分子中碳原子轨道杂化类型从左到右,第一、第二个C原子的杂化为sp2杂化,第三个C原子的杂化是sp杂化。分子中处于同一直线上的原子数目最多为 3个。
。由O22+的电子式可知在每个O22+中含有2个Π,在1molO22+中含有的Π键数目为2NA。(4)由CaC2晶体的晶胞结构可看出在CaC2晶体中1个Ca2+周围距离最近的C22-数目为4个。(5)Cu是29号元素,其Cu+基态核外电子排布式为1s22s22p63s23p63d10
。 (6)在丙烯腈分子中碳原子轨道杂化类型从左到右,第一、第二个C原子的杂化为sp2杂化,第三个C原子的杂化是sp杂化。分子中处于同一直线上的原子数目最多为 3个。
考点:考查乙炔的分子结构、化学性质、组成元素的电离能的比较及形成的化合物丙烯晴等的结构的知识。


科目:高中化学 来源: 题型:
 (2010?江苏)乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.
(2010?江苏)乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.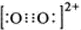
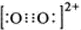
查看答案和解析>>
科目:高中化学 来源: 题型:

| C | 2- 2 |
| O | 2+ 2 |
| O | 2+ 2 |
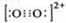
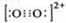
| O | 2+ 2 |
| C | 2- 2 |
| C | 2- 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| C | 2- 2 |
| O | 2+ 2 |
| O | 2+ 2 |
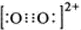
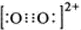
| O | 2+ 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
乙炔是有机合成工业的一种原料。工业上曾用![]() 与水反应生成乙炔。
与水反应生成乙炔。
(1) 将乙炔通入![]() 溶液生成
溶液生成![]() 红棕色沉淀。
红棕色沉淀。![]() 基态核外电子排布式为 。
基态核外电子排布式为 。
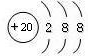
(2) Ca2+的原子结构示意图: ;已知![]() 中
中![]() 与
与![]() 互为等电子体,
互为等电子体,![]() 的电子式可表示为 ;1mol
的电子式可表示为 ;1mol ![]() 中含有的
中含有的![]() 键数目为 。
键数目为 。
(3)乙炔与氢氰酸反应可得丙烯腈![]() 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
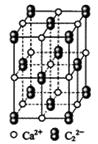
(4) ![]() 晶体的晶胞结构与
晶体的晶胞结构与![]() 晶体的相似(如右图所示),但
晶体的相似(如右图所示),但![]() 晶体中含有的哑铃形
晶体中含有的哑铃形![]() 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。![]() 晶体中1个
晶体中1个![]() 周围距离最近的
周围距离最近的![]() 数目为 。
数目为 。
查看答案和解析>>
科目:高中化学 来源:2010年黑龙江省高二下学期期末考试化学试题 题型:填空题
(7分)乙炔是有机合成工业的一种原料。工业上曾用 与水反应生成乙炔。
与水反应生成乙炔。
(1) 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
;1mol
的电子式可表示为
;1mol  中含有的
中含有的 键数目为_
。
键数目为_
。
(2)将乙炔通入 溶液生成
溶液生成 ,红棕色沉淀。
,红棕色沉淀。 基态核外电子排布式为
。
基态核外电子排布式为
。
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为_ 。
(4) 晶体的晶胞结构与
晶体的晶胞结构与 晶体的相似(如右图所示),但
晶体的相似(如右图所示),但 晶体中含有的中哑铃形
晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。 晶体中1个
晶体中1个 周围距离最近的
周围距离最近的 数目为_
。
数目为_
。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com