
 (2010?江苏)乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.
(2010?江苏)乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.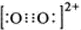
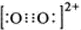
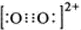 ,在1个O22+含有2个π键,故1 mol O22+中,含有2NA个 π键,故答案为:
,在1个O22+含有2个π键,故1 mol O22+中,含有2NA个 π键,故答案为: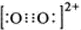 ;2NA;
;2NA;

科目:高中化学 来源: 题型:
(2010?江苏)在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ?mol-1)
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 5.6-1.4 |
| 56 |
| 32.29 |
| 143.5 |
| n(Fe) |
| n(Cl) |
| 1 |
| 3 |
| 5.6-1.4 |
| 56 |
| 32.29 |
| 143.5 |
| n(Fe) |
| n(Cl) |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2010?江苏二模)近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.
(2010?江苏二模)近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.| 25 |
| 2 |
| 25 |
| 2 |
| 放电 |
| 充电 |
| 1 |
| 2 |
| 容器编号 | c(CO)/mol?L-1 | c (02)/mol?L-1 | c (C02)/mol?L-1 | v(正)和v (逆)比较 |
| I | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||


查看答案和解析>>
科目:高中化学 来源: 题型:
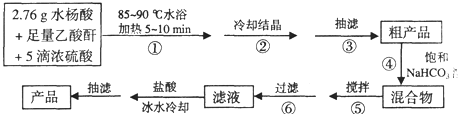
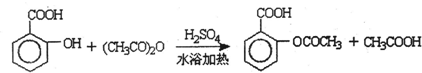
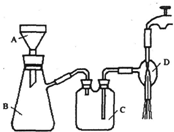
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com