(2010?江苏二模)近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.
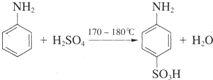
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C
8H
18计)和氧气充分反应,每生成1mol水蒸气放热569.1kJ.则该反应的热化学方程式为
C
8H
18(l)+
O
2(g)=8CO
2(g)+9H
2O(g)△H=-5121.9kJ?mol
-1C
8H
18(l)+
O
2(g)=8CO
2(g)+9H
2O(g)△H=-5121.9kJ?mol
-1.
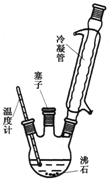
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理示意如图,其总反应式是:H
2+2N
iOOH
2N
i(OH)
2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将
增大
增大
(填“增大”、“不变”或“减小”),该电极的电极反应式为
NiOOH+H2O+e-=Ni(OH)2+OH-
NiOOH+H2O+e-=Ni(OH)2+OH-
.
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:CO(g)+
O
2(g)?CO
2(g).
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.
| 容器编号 |
c(CO)/mol?L-1 |
c (02)/mol?L-1 |
c (C02)/mol?L-1 |
v(正)和v (逆)比较 |
| I |
2.0×10-4 |
4.0×10-4 |
4.0×10-2 |
v(正)=v(逆) |
| Ⅱ |
3.0×10-4 |
4.0×10-4 |
5.0×10-2 |
|
②相同温度下,某汽车尾气中CO、CO
2的浓度分别为1.0×10
-5mol?L
-1和1.0×10
-4mol?L
-1.若在汽车的排气管上增加一个补燃器,不断补充O
2并使其浓度保持为1.0×10
-4mol?L
-1,则最终尾气中CO的浓度为
1.1×10-6
1.1×10-6
mol?L
-1.

 (2010?江苏二模)近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.
(2010?江苏二模)近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态. CO2(g).
CO2(g).

 阅读快车系列答案
阅读快车系列答案