
| A、Fe(OH)2 |
| B、Fe(OH)3 |
| C、CaSiO3 |
| D、Fe(NO3)3 |
| ||


科目:高中化学 来源: 题型:
 锌与不同浓度的硫酸反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为101kPa,温度为0℃):
锌与不同浓度的硫酸反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为101kPa,温度为0℃):| a |
| 65 |
| b |
| 64+V |
| V |
| 22400 |
| n(H2) |
| n(SO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
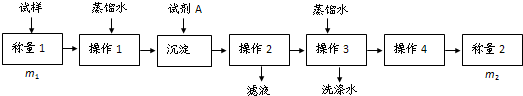
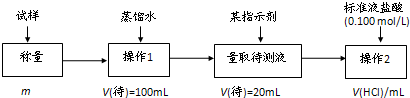
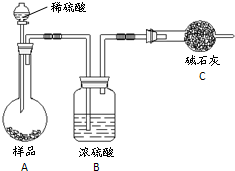
查看答案和解析>>
科目:高中化学 来源: 题型:

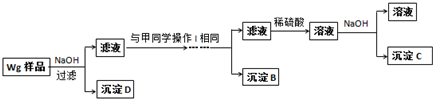
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、.该反应是吸热反应 |
| B、该反应是放热反应 |
| C、铁粉和硫粉在常温下难以发生反应,加热才反应,所以该反应△H>0 |
| D、生成物硫化亚铁的总能量高于反应物铁粉和硫粉的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com