
在某锂离子电池中,有一种有机聚合物作为 正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:
正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:
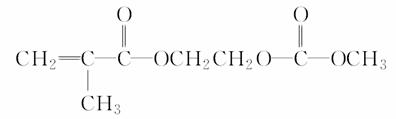
用相对分子质量为56的单烯烃A合成M的方法可设计如下:

请回答下列问题:
(1)A的结构简式是______________________________________________________,
试剂Ⅱ是__________________,反应Ⅲ的化学反应类型是__________________。
(2)G在一定条件下反应生成的高聚物是制备隐形眼镜的材料,请写出生成该高聚物的化学反应方程式__________________________________________________________。
(3)M与足量氢氧化钠溶液反应的化学方程式是_______________________________
________________________________________________________________________。
(4)在用E制备F的过程中,2分子的E反应会生成一种副产物,其核磁共振氢谱只有一种吸收峰,该副产物的结构简式为_________________________________________。
科目:高中化学 来源: 题型:
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
A.异戊二烯( )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B.2氯丁烷(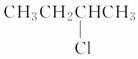 )与NaOH的乙醇溶液共热发生消去HCl分子的反应
)与NaOH的乙醇溶液共热发生消去HCl分子的反应
C.甲苯在一定条件下发生硝化,生成一硝基甲苯的反应
D.邻羟基苯甲酸与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,X的单质只有氧化性.
(1)写出实验室制取W2反应的离子方程式 .
(2)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究YX2和W2的性质.

①分别通入YX2和W2,在装置A中观察到的现象是否相同(填“相同”或“不相同”) ;若装置D中装的是铁粉,当通入W2时D中观察到的现象为 ;若装置D中装的是五氧化二钒,当通入YX2时,打开K通入适量X2,化学反应方程式为 ;
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,则该反应的化学方程式为 .
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量(填字母) ,可以看到白色沉淀生成,其原因为 ______________________(写出其中一种即可).
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙
(4)若由元素Y和X组成—2价酸根Z,Z中Y和X的质量比为Y:X=4:3,当W2与含Z的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生.写出W2与Z的溶液完全反应产生浅黄色沉淀的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的k^s5*u方法错误的k^s5*u是( )
A.蒸馏常用于分离提纯液态有机混合物
B.对有机物分子红外光谱图的k^s5*u研究有助于确定有机物分子中的k^s5*u官能团
C.燃烧法是研究确定有机物成分的k^s5*u有效方法
D.核磁共振氢常用于分析有机物的k^s5*u相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
①写出有机物(a)的系统命名法的名称 。
②有机物(a)有一种同分异构体,试写出其结构简式
。
③上述有机物中与(c)互为同分异构体的是 (填代号)。
④与(e)互为同系物的最简单有机物的结构简式为:
。
⑤上述有机物中不能与溴水反应使其褪色的有 (填代号)。
⑥(d)与氯气发生1,4加成的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:


下列有关叙述正确的是
A.贝诺酯分子中有三种含氧官能团
B.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D.贝 诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示物质制备的方法中正确的是( )
A.NaCl(饱和溶液) HCl
HCl
B.Cu CuSO4溶液
CuSO4溶液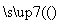
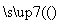 CuSO4·5H2O晶体
CuSO4·5H2O晶体
C.MnO2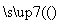 Cl2
Cl2
D.C6H6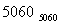 硝基苯
硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室以含有Ca2+、Mg2+、Cl-、SO 、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如
、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如 下:
下:
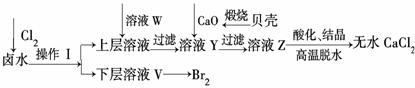
(1)操作Ⅰ使用的试剂是________,所用主要仪器的名称是________。
(2)加入溶液W的目的是________。用CaO调节溶液Y的pH,可以除去Mg2+。由表中数据可知,理论上可选择的pH最大范围是________。酸化溶液Z时,使用的试剂为________。
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8 mol·L-1 |
(3)实验室用贝壳与稀盐酸反应制备并收集CO2气体,下列装置中合理的是________。

(4)常温下,H2SO3的电离常数Kal=1.2×10-2,Ka2=6.3×10-3,H2CO3的电离常数Kal=4.5×10-7,Ka2=4.7×10-11。某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于________。
设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论):________________________。仪器自选。
供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏伽德罗常数,下列说法正确的是
A.1mol Mg Cl2中含有的离子数为2NA‘
B.标准状况下,11.2L H2O中含有的原子数为1.5NA
C.标准状况下,22.4L氦气与22.4L氯气所含原子数均为2NA
D.常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com