
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A、反应在t1 min内的平均速率为v(H2)=
| ||
| B、保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率不变,H2O的体积分数不变 | ||
| C、保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)=0.40 mol | ||
| D、温度升高至800℃,上述反应平衡常数为0.64,则正反应为放热反应 |
| △n/V |
| △t |
| 0.4mol/2L |
| t 1min |
| 0.2 |
| t ! |
| 0.2 |
| t1 |
| 0.4×0.4 |
| 0.8×0.2 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、自然界硅元素的贮量丰富 |
| B、硅可用于制造光导纤维 |
| C、高纯度的单质硅被广泛用于制作计算机芯片 |
| D、硅可由二氧化硅还原制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:
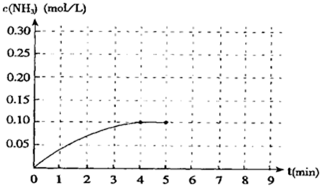
查看答案和解析>>
科目:高中化学 来源: 题型:
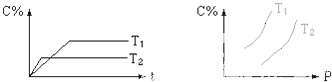
| A、正反应是吸热反应 |
| B、m+n<e |
| C、逆反应是放热反应 |
| D、m+n>e |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、被其他卤素单质从其卤化物中置换出来的可能性随核电荷数的增加而增大 |
| B、单质的颜色随核电荷数的增加而加深 |
| C、它们的原子核外电子层数随核电荷数的增加而增多 |
| D、它们的氢化物的稳定性随核电荷数的增加而增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V(O2)=0.01mol?L-1?s-1 |
| B、V(NO)=0.008mol L-1?s-1 |
| C、V(H2O)=0.015mol L-1?s-1 |
| D、V(NH3)=0.002mol L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com