


科目:高中化学 来源: 题型:
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A、反应在t1 min内的平均速率为v(H2)=
| ||
| B、保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率不变,H2O的体积分数不变 | ||
| C、保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)=0.40 mol | ||
| D、温度升高至800℃,上述反应平衡常数为0.64,则正反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
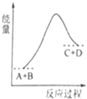
| A、当A的正反应速率与C的逆反应速率相同时处于平衡状态 |
| B、当A、B、C、D的浓度相同时,反应处于平衡状态 |
| C、反应物的总键能量低于生成物的总键能 |
| D、该反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、还原性:Na>Mg>Al>Fe |
| B、碱性:Al(OH)3>Mg(OH)2 |
| C、稳定性:HF>HCl>HBr>HI |
| D、酸性:HClO4>H2SO4>CH3COOH>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 点燃 |
| 点燃 |
| A、减小空气进入量,减小石油气进入量 |
| B、增大空气进入量或减小石油气进入量 |
| C、增大空气进入量,增大石油气进入量 |
| D、减小空气进入量或增大石油气进入量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在100 mL 1 mol?L-1的 Fe(NO3)3的溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ |
| B、在100 mL 2 mol?L-1的FeI2的溶液中通入标况下5.6 L的Cl2:4Fe2++6I-+5Cl2═4Fe3++3I2+10Cl- |
| C、向NaHCO3溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| D、向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3HCl+Fe(OH)3═FeCl3+3H2O |
| B、HNO3+KOH═KNO3+H2O |
| C、H2SO4+Ba(OH)2═BaSO4↓+2H2O |
| D、2HCl+Cu(OH)2═CuCl2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com