
| A. | 液氨可用作制冷剂 | |
| B. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| C. | 用带磨口玻璃塞的试剂瓶盛放Na2CO3溶液 | |
| D. | 光纤通信的光导纤维是由石英经特殊工艺制成的 |
分析 A.液氨气化吸热;
B.燃煤脱硫技术,可减少二氧化硫的排放;
C.二氧化硅与碱性溶液反应生成具有粘合性的硅酸钠;
D.石英的主要成分为二氧化硅,二氧化硅对光具有良好的全反射作用.
解答 解:A.液氨气化吸热,导致周围温度降低,则可用作制冷剂,故A正确;
B.燃煤脱硫技术,可减少二氧化硫的排放,防止酸雨发生,故B正确;
C.二氧化硅与碱性溶液反应生成具有粘合性的硅酸钠,则用橡皮塞的试剂瓶盛放Na2CO3溶液,故C错误;
D.石英的主要成分为二氧化硅,二氧化硅对光具有良好的全反射作用,则光纤通信的光导纤维是由石英经特殊工艺制成的,故D正确;
故选C.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 五种元素中有两种金属元素 | |
| B. | 元素C、D、E的最高价氧化物对应水化物的酸性增强 | |
| C. | 元素D、E分别与元素A形成化合物的稳定性:A2D>AE | |
| D. | 元素B、D、E的简单离子半径大小为:B>D>E |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{62}^{144}$Sm和${\;}_{62}^{150}$Sm是同一种核素 | |
| B. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的质量数相同 | |
| C. | ${\;}_{62}^{144}$Sm和${\;}_{62}^{150}$Sm互为同位素 | |
| D. | ${\;}_{62}^{144}$Sm和${\;}_{62}^{150}$Sm的核外电子数和中子数均为62 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素C昜被氧化,当新鲜蔬菜煮熟后,所含维生素C会有所损失 | |
| B. | 钢筋混凝土属复合材料 | |
| C. | 光导纤维和计算机芯片的主要材料都是单质硅 | |
| D. | 生产水泥、玻璃、熟石灰都要用到石灰石这一原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L的HCl 95mL | B. | 0.2mol/L的HCl 90mL | ||
| C. | 0.15mol/L的H2SO410mL | D. | 18mol/L的H2SO485mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 氯化硼中心原子采用sp杂化 | |
| C. | 氯化硼分子与氯化铝分子互为等电子体,都是非极性分子 | |
| D. | 氯化硼的熔沸点与氯硼键的键能大小有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷>乙烷>甲烷 | B. | 邻二甲苯>间二甲苯>对二甲苯 | ||
| C. | 正戊烷>异戊烷>新戊烷 | D. | 对二甲苯>邻二甲苯>间二甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1molNa2O2与水反应转移电子数目为0.1NA | |
| B. | 1mol金刚石中含C-C数目为4 NA | |
| C. | 标况下2.24升Cl2含孤电子对的数目为0.2 NA | |
| D. | PH=2的盐酸溶液中H+的数目为0.01 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
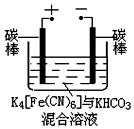 材料一:连二亚硫酸钠(Na2S2O4)是一种常用还原剂,俗称保险粉.工业制备方法如下:
材料一:连二亚硫酸钠(Na2S2O4)是一种常用还原剂,俗称保险粉.工业制备方法如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com