
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物。试回答下列问题:
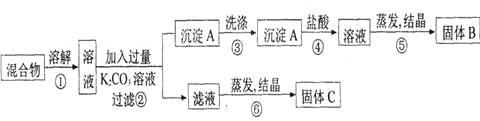
(1)B物质的化学式为_____________________。
(2)该方案的明显失误是因某一步设计不当而使分离产物不纯,该步骤是_______(填序号)改进措施是__________________________。
(3)写出K2CO3的电离方程式_________________________________________________。
(4)写出②④两步中对应的离子方程式:
②_______________________________________________________________
④_______________________________________________________________
【答案】BaCl2 ⑥ 在步骤⑥蒸发结晶之前向滤液中滴加盐酸至不再冒气泡( K2CO3 =2K++CO32- Ba2++CO32-= BaCO3↓ BaCO3+2H+=Ba2+CO2↑+H2O
【解析】
混合物溶解所得溶液中加入K2CO3过滤得沉淀A为BaCO3,滤液为KCl和过量的K2CO3的混合液,蒸发结晶得固体C为KCl ,此过程应用适量的HCl除去过量的K2CO3,沉淀A用盐酸溶解得BaCl2溶液,蒸发结晶得固体B为BaCl2。
(1)从以上分析可知,B为BaCl2溶液,故答案为BaCl2;
(2)KCl和BaCl2的混合液中加入过量的K2CO3溶液后,得到沉淀BaCO3和滤液KCl和过量的K2CO3的混合液,直接蒸发结晶,得到的KCl中会混有K2CO3,所以在步骤⑥蒸发结晶之前向滤液中滴加盐酸至不再冒气泡以除去K2CO3,故答案为:⑥,步骤⑥蒸发结晶之前向滤液中滴加盐酸至不再冒气泡;
(3)K2CO3是强电解质,完全电离,其电离方程式为:K2CO3 =2K++CO32-;
(4)第②步反应是BaCl2和K2CO3反应:Ba2++CO32-= BaCO3↓;第④步是BaCO3和HCl反应:BaCO3+2H+=Ba2+CO2↑+H2O。


科目:高中化学 来源: 题型:
【题目】一定量氢气在氯气中燃烧,所得混合物用![]() 溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。
溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。
(1)所得混合物与NaOH溶液反应的离子方程式______
(2)所得溶液中NaCl的物质的量为________。
(3)所用氯气和参加反应的氢气的物质的量之比![]() ________。
________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】创建文明校园,学校全园禁烟,同学们也参与了“寻找烟头”活动。吸烟有害健康,烟草中的剧毒物尼古丁的结构简式为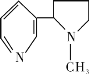 ,有关其叙述正确的是
,有关其叙述正确的是
A. 该有机物属于芳香族化合物
B. 尼古丁分子中的C、N原子均处于同一平面内
C. 尼古丁分子中的六元环不是正六边形
D. 尼古丁的一氯代物有10种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是新型灭菌消毒剂,实验室通常用以下方法制得该气体:2KClO3+H2C2O4+ H2SO4 ![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
A.1 mol KClO3参与反应转移1 mol电子B.KClO3在该反应中被氧化
C.H2C2O4的还原性强于ClO2D.CO2是氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.19 g/mL、质量分数为36.5%的浓盐酸配制500 mL 0.4 mol/L盐酸。回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为______。
(2)欲用上述浓盐酸和蒸馏水配制500 mL 0.4 mol/L盐酸。
①需量取______mL上述浓盐酸进行配制。
②该配制实验中所需要的主要玻璃仪器有量筒、烧杯、玻璃棒、_____________。
③用上述浓盐酸配制0.4 mol/L盐酸,定容的操作是_____________________。
(3)配制500 mL 0.4 mol/L盐酸时,下列操作中会导致结果偏低的是____________(填序号)。
a.用量筒量取浓盐酸时仰视量筒的刻度
b.用量筒量取浓盐酸后洗涤量筒,并把洗涤液转入容量瓶中
c.摇匀后发现液面低于刻度线,又加水至刻度线
d.将所配制溶液从容量瓶转移到试剂瓶中时,有少量液体溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硅晶体是立体的网状结构,其结构如图所示。关于二氧化硅的下列说法中,不正确的是( )

A. 晶体中Si、O原子个数比为1∶2
B. 晶体中最小原子环上的原子数为8
C. 晶体中最小原子环上的原子数为12
D. 晶体中Si、O原子最外层都满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]![]() 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
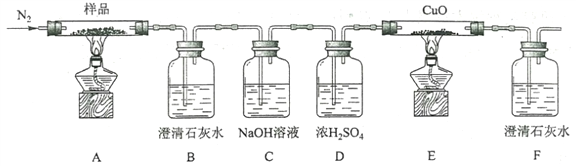
①通入氮气的目的是________________________________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________、___________。
③为防止倒吸,停止实验时应进行的操作是_____________________________。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。

(1)A是铅蓄电池的___________极,铅蓄电池正极反应式为___________,放电过程中电解液的密度___________ (填“减小”、“增大”或“不变”)。
(2)Ag电极的电极反应式是___________,该电极的电极产物共____________g。
(3)Cu电极的电极反应式是____________,CuSO4溶液的浓度____________(填“减小”、“增大”或“不变”)
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示___________。

a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 I.依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)设计的原电池如图所示。
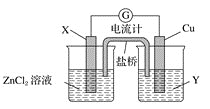
请回答下列问题:
(1)铜电极为电池的________极;电解质溶液Y是________________。
(2)盐桥中的Cl-向________(填“左”、或“右”)移动,如将盐桥撤掉,电流计的指针将不偏转。
Ⅱ.电解原理在化学工业中有广泛应用。
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题:
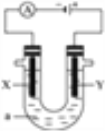
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是_________________;
②电解一段时间后,该反应总离子方程式_______________________________;
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是____________电解一段时间后,CuSO4溶液浓度_________(填“增大”、减小”或“不变”)。
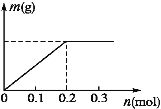
(3)若X、Y都是惰性电极,a是溶质为Cu(NO3)2和X(NO3)3,且均为0.1 mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com