
下列不能形成配位键的组合是( )
|
| A. | Ag+、NH3 | B. | BF3、NH3 | C. | Co3+、CO | D. | Ag+、H+ |
考点:
配合物的成键情况.
专题:
化学键与晶体结构.
分析:
根据配位键形成的条件,一方要提供空轨道,另一方提供孤电子对,据此答题;
解答:
解:根据配位键形成的条件,一方要提供空轨道,另一方提供孤电子对,
A、Ag+有空轨道,NH3中的氮原子上的孤电子对,可以形成配位键,故A错误;
B、BF3中B原子有空轨道,NH3中的氮原子上的孤电子对,可以形成配位键,故B错误;
C、Co3+有空轨道,CO中的氧原子上的孤电子对,可以形成配位键,故C错误;
D、Ag+、H+两种离子者没有孤电子对,所以不能形成配位键,故D正确;
故选D.
点评:
本题主要考查配位键形成的条件,难度较小,解题时要注意弄清楚各种原子或离子的最外层电子对的情况.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
通常把原子总数和价电子总数相同的分子或离子称为等电子体.人们发现等电子体的空间结构相同,则下列有关说法中正确的是( )
|
| A. | CH4和NH4+是等电子体,键角均为60° |
|
| B. | B3N3H6和苯是等电子体,1molB3N3H6和苯均有6mol非极性键 |
|
| C. | NH3和PCl3是等电子体,均为三角锥形结构 |
|
| D. | BF3和CO32﹣是等电子体,均为平面正三角形结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(X代表卤素原子,R代表烃基)
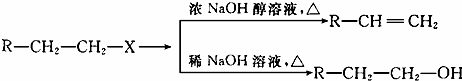
利用上述信息,按以下步骤从 合成
合成 .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去)

请回答下列问题:
(1)分别写出B、D的结构简式:B _、D .
(2)反应①~⑦中属于消去反应的是 .(填数字代号)
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为: .
(4)试写出C→D反应的化学方程式(有机物写结构简式,并注明反应条件): .
查看答案和解析>>
科目:高中化学 来源: 题型:
木糖醇常用做口香糖的甜味剂.木糖醇的结构简式为CH2OH﹣CHOH﹣CHOH﹣CHOH﹣CH2OH,下列有关木糖醇的说法不正确的是( )
|
| A. | 是一种单糖 | B. | 能发生酯化反应 |
|
| C. | 不能发生水解反应 | D. | 在口腔中不易被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氢键,下列说法正确的是( )
|
| A. | 每一个水分子内含有两个氢键 |
|
| B. | 冰、水和水蒸气中都存在氢键 |
|
| C. | DNA中的碱基互补配对是通过氢键来实现的 |
|
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种短周期元素,它们的结构、性质等信息如下表所述.
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式 .
(2)B元素在周期表中的位置 ;离子半径:B A(填“大于”或“小于”).
(3)C原子的价电子排布图是 ,其原子核外有 个未成对电子,能量最高的电子为 轨道上的电子,其轨道呈 形.C的气态氢化物极易溶于水的原因是 ;与C的单质互为等电子体的分子的结构式 .
(4)D﹣的结构示意图是 .
(5)B的最高价氧化物对应的水化物与D的最高价氧化物的水化物反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )

|
| A. | 原子半径:Z>Y>X |
|
| B. | 气态氢化物的稳定性:R>W |
|
| C. | WX3和水反应形成的化合物是离子化合物 |
|
| D. | Y和Z两者最高价氧化物对应的水化物不能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液含有K+、Fe3+、SO42﹣、CO32﹣、I﹣中的几种.取样,滴加KSCN溶液后显血红色.为确定该溶液的组成,还需检验的离子是( )
A.K+
B.I﹣
C.SO42﹣
D.CO32﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com