
分类是化学学习与研究的常用方法,下列分类正确的是( )\
A.非金属氧化物均属于酸性氧化物
B.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
C.根据电解质的水溶液导电性的强弱,将电解质分为强电解质和弱电解质
D.根据反应物和生成物的类别以及反应前后物质种类的多少,把化学反应分为化合反应、分解反应、置换反应和复分解反应
考点:
酸、碱、盐、氧化物的概念及其相互联系;分散系、胶体与溶液的概念及关系;化学基本反应类型;强电解质和弱电解质的概念..
专题:
物质的分类专题.
分析:
A、有些非金属氧化物不是酸性氧化物;
B、分散系分为溶液、浊液和胶体的依据是微粒直径大小;
C、电解质水溶液中是否完全电离分类为强电解质和弱电解质;
D、根据反应物和生成物的类别以及反应前后物质种类的多少,化学反应分为四种基本类型.
解答:
解:A、有些非金属氧化物不是酸性氧化物,CO、NO、H2O属于不成盐氧化物,故A错误;
B、分散系分为溶液、浊液和胶体的依据是微粒直径大小,否具有丁达尔效应,区分溶液和胶体,故B错误;
C、电解质水溶液中是否完全电离分类为强电解质和弱电解质,强电解质溶液导电性不一定强于弱电解质,故C错误;
D、根据反应物和生成物的类别以及反应前后物质种类的多少,化学反应分为四种基本类型,分为化合反应、分解反应、置换反应和复分解反应,故D正确;
故选D.
点评:
本题考查了物质分类方法,分散系本质特征,电解质性质的理解应用,反应类别分类方法,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:
下列说法正确的是
A.乙醇和乙酸都能与金属钠反应
B.淀粉水解的最终产物是氨基酸
C.植物油和动物脂肪都不能使溴水褪色
D.苯、乙烯都能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在密闭容器中可逆反应.N2(g)+3H2(g)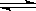 2NH3(g)达到平衡状态,此时N2的转化率为20%,H2的转化率为50%,则平衡时体系的压强为反应前的( )
2NH3(g)达到平衡状态,此时N2的转化率为20%,H2的转化率为50%,则平衡时体系的压强为反应前的( )
A.1/5 B.3/4 C.9/11 D.1/2
查看答案和解析>>
科目:高中化学 来源: 题型:
从对化合物分类方法出发,指出下列各组物质中与其他物质类型不同的一种物质。
A.Na2O、CaO、SO2、CuO________。
B.NaCl、KCl、NaClO3、CaCl2________。
C.HClO3、KClO3、HCl、NaClO3________。
D.NaHCO3、Ca(HCO3)2、NH4HCO3、K2CO3________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | FeCl3 溶液与铁反应:Fe+Fe3+═2Fe2+ |
|
| B. | 向Ca(HCO3)2溶液中加入足量NaOH溶液:Ca2++HCO3﹣+OH﹣=CaCO3↓+H2O |
|
| C. | 铝粉溶于NaOH溶液中:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑ |
|
| D. | 金属钠跟水反应Na+2H2O═Na++OH﹣+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是( )
|
| A. | 硫酸的摩尔质量是98g |
|
| B. | 1mol氧的质量等于16g |
|
| C. | 摩尔是一个基本物理量 |
|
| D. | 12g 12C所含原子数称为阿伏加德罗常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一次化学研究性学习实验中,某研究小组学生,研究分析某两瓶无标签的试剂,只知道一瓶是固体,另一瓶是液体,取少量两种试剂在试管中混合,立即产生一种无色无味的气体.现请你对此气体开展一系列探究,并完成下列实验报告.
(1)①此气体是什么物质(只写出其中可能的一种)?验证它的实验方案如下:
| 猜想 | 实验步骤 | 现象及结论 |
| 此气体可能是 氧气 | 将带火星的木条伸入集气瓶中 | __ 木条复燃,则证明是氧气 |
产生此气体的化学方程式可能是 2H2O2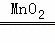 2H2O+O2↑
2H2O+O2↑
②想制取该气体(用本题中两瓶无标签的试剂),采用的发生装置可选用下图A、B、C中的 B (对应填序号).
收集该气体可选用D中的 b 装置.
③若图E是收集该气体的装置,气体由 a 端(填“a”或“b”)导入.
(2)猜想此无色气体还有无可能是另一种气体,如果有,请写出产生它的化学方程式 CaCO3+2HCl=CaCl2+H2O+CO2↑ (只须写一种).

查看答案和解析>>
科目:高中化学 来源: 题型:
高富氧底吹熔池炼铜新工艺反应炉如图
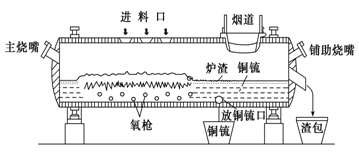
(1)该新工艺的优点之一是混合矿料不需要干燥、磨细。烟气进入余热锅炉后,经静电除尘后进入酸厂回收利用,这样做体现化学的________思想。
(2)该新工艺的优点之二是首次投料需要添加少量的燃料,当反应充分启动后就不需要再投放燃料,说明反应炉中的反应总体来说是________反应。
(3)此法冶炼的矿石主要是黄铜矿(主要成分是CuFeS2),经过上面设备煅烧后最终化合态的铜生成铜和SO2,在冶炼铜矿过程中存在重要反应:2CuFeS2+O2=Cu2S+2FeS+SO2、2Cu2S+3O2=2Cu2O+2SO2、________________________________。
(4)从放铜锍口放出的铜锍中还含有铁和硫必须除去,铜锍吹炼过程是火法冶炼生产粗铜的最后一道工序,吹炼过程分为两个阶段。第一阶段的任务是使铁氧化造渣,主要化学反应为:①2FeS+3O2+SiO2=2FeO·SiO2+2SO2 ,第二阶段是使上一个阶段中没有反应彻底的Cu2S氧化成粗铜,主要化学反应为:②Cu2S+O2=2Cu+SO2,下列关于反应①、②的分析正确的是________(填序号)
A.反应②氧化剂只有O2
B.硫元素在①和②均被氧化
C.①和②在反应过程中都有共价键破坏和共价键形成
(5)图中渣包中的炉渣含有Fe2O3、FeO 、SiO2等,选用提供的试剂设计实验验证炉渣中含有FeO。提供的试剂:KMnO4溶液、KSCN溶液、NaOH溶液、稀硫酸、稀盐酸,所选试剂为_______________。实验现象是__________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com