
【题目】聚合物 L(![]() )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如图:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如图:

已知:①C、D、K 均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels﹣Alder 反应![]() +
+![]()
![]()
![]()
③ R2Cl![]() R1OR2
R1OR2
(1)I→J 的反应类型是________,D 的名称是________,G 中所含官能团的名称是________。
(2)B 的结构简式是________,“B→C”的反应中,除 C 外,另外一种产物是________。
(3)D+K→L 的化学方程式是________。
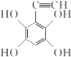
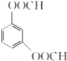
(4)M 为 D 的同分异构体,同时满足下列条件的 M 的结构简式为________。
①1 molM 最多消耗 4 mol NaOH ②核磁共振氢谱有 4 组吸收峰
(5)N 是 D 的同系物,相对分子质量比 D 大 14,则 N 可能的结构有________种。
(6)已知:乙炔与 1,3﹣丁二烯也能发生 Diels﹣Alder 反应。请以 1,3﹣丁二烯和乙炔为原料,选用必要的无机试剂合成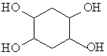 ,写出合成路线:________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线:________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
【答案】还原反应 对苯二甲酸 醚键 ![]() H2O
H2O 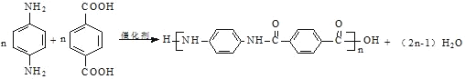
 、
、 10
10 ![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
乙醇发生消去反应生成A为CH2=CH2,C被氧化生成D,D中含有羧基,C、D、K 均为芳香族化合物,分子中均只含两种不同化学环境的氢原子,C发生氧化反应生成D,D中应该有两个羧基,根据L结构简式知,D为![]() 、K为
、K为![]() ;根据信息②知,生成B的反应为加成反应,B为
;根据信息②知,生成B的反应为加成反应,B为![]() ,B生成C的反应中除了生成C外还生成H2O;H为
,B生成C的反应中除了生成C外还生成H2O;H为![]() ,根据信息③知,G为
,根据信息③知,G为![]() ,F为
,F为![]() ,根据F,可知E为苯;H经过硝化反应得到I,则I为
,根据F,可知E为苯;H经过硝化反应得到I,则I为![]() ,据此分析作答。
,据此分析作答。
(1) I为![]() ,J为
,J为![]() ,则I→J 的反应类型是还原反应;D为
,则I→J 的反应类型是还原反应;D为![]() ,其名称是对苯二甲酸;G为
,其名称是对苯二甲酸;G为![]() ,所含官能团的名称是醚键,故答案为:还原反应;对苯二甲酸;醚键;
,所含官能团的名称是醚键,故答案为:还原反应;对苯二甲酸;醚键;
(2)乙烯和![]() 发生Diels-Alder反应生成B,故B的结构简式是
发生Diels-Alder反应生成B,故B的结构简式是![]() ;C为芳香族化合物,分子中只含两种不同化学环境的氢原子,“B→C”的反应中,除C外,还生成的一种无机产物是H2O,故答案为:
;C为芳香族化合物,分子中只含两种不同化学环境的氢原子,“B→C”的反应中,除C外,还生成的一种无机产物是H2O,故答案为:![]() ;H2O;
;H2O;
(3) D为![]() ,K为
,K为![]() ,L为
,L为![]() ,则D+K→L 的化学方程式是:
,则D+K→L 的化学方程式是: ,故答案为:
,故答案为: ;
;
(4) D为![]() ,M 为 D 的同分异构体,满足①1 molM最多消耗 4 mol NaOH,说明苯环上的取代基为4个酚羟基和一个乙炔基或为两个-OOCH;②核磁共振氢谱有 4 组吸收峰,说明存在四种氢,满足的有:
,M 为 D 的同分异构体,满足①1 molM最多消耗 4 mol NaOH,说明苯环上的取代基为4个酚羟基和一个乙炔基或为两个-OOCH;②核磁共振氢谱有 4 组吸收峰,说明存在四种氢,满足的有: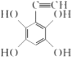 、
、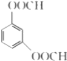 ,故答案为:
,故答案为: 、
、 ;
;
(5) D为![]() ,N是D的同系物,相对分子质量比D大14,如果取代基为CH2COOH、COOH,有3种结构;如果取代基为CH3、两个COOH,有6种结构;如果取代基为CH(COOH)2,有1种,则符合条件的有10种,故答案为:10;
,N是D的同系物,相对分子质量比D大14,如果取代基为CH2COOH、COOH,有3种结构;如果取代基为CH3、两个COOH,有6种结构;如果取代基为CH(COOH)2,有1种,则符合条件的有10种,故答案为:10;
(6) CH2=CHCH=CH2和HC≡CH发生加成反应生成![]() ,
,![]() 和溴发生加成反应生成
和溴发生加成反应生成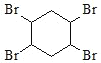 ,
, 发生水解反应生成
发生水解反应生成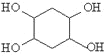 ,其合成路线为
,其合成路线为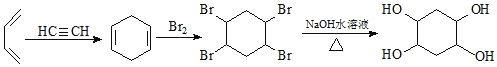 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】已知Al2H6燃烧热极高,是一种很好的生氢剂,它跟水反应生成H2,球棍模型如图(白球为Al,黑球为H).下列推测肯定不正确的是( )

A. 该物质与水反应,属于氧化还原反应
B. Al2H6在空气中完全燃烧,产物为氧化铝和水
C. Al2H6分子中 氢为+1价,铝为﹣3价
D. 氢铝化合物可能成为未来的储氢材料和火箭燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是373K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是 ( )
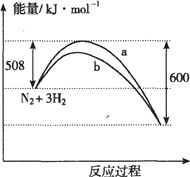
A. 该反应的热化学方程式为:N2+3H2![]() 2NH3 △H=-92kJ·mol-1
2NH3 △H=-92kJ·mol-1
B. 加入催化剂,该化学反应的反应热不变
C. a曲线是加入催化剂时的能量变化曲线
D. 在温度体积一定的条件下,通入1mol N2和3 mol H2反应后放出的热量为Q1kJ,则Q1=92
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1
2CO(g)+O2(g)===2CO2(g) ΔH2
2H2(g)+O2(g)===2H2O(g) ΔH3
则反应CO(g)+2H2(g)===CH3OH(g)的ΔH=______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。

①T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
②由CO合成甲醇时,CO在250 ℃、300 ℃、350 ℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为________ ℃。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是____________。

③以下有关该反应的说法正确的是________(填序号)。
A.恒温、恒容条件下,若容器内的压强不再发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2 mol CO和6 mol H2充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(3)一定温度下,向2 L固定体积的密闭容器中加入1 mol CH3OH(g),发生反应:CH3OH(g) ![]() CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。

0~2 min内的平均反应速率v(CH3OH)=__________。该温度下,反应CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g)
CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g) ![]() CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组以废弃的易拉罐、漂白粉、氢氧化钠等为原料制造了一种新型环保电池,并进行相关实验,如图所示。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO![]() +H2O。下列说法正确的是
+H2O。下列说法正确的是
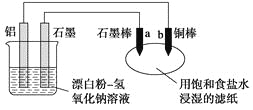
A. 电池的负极反应式为:ClO-+H2O+2e-=Cl-+2OH-
B. 当有0.1 mol Al完全溶解时,流经电解液的电子数为1.806×1023个
C. 往滤纸上滴加酚酞试液,b极附近颜色变红
D. b极附近会生成蓝色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
①氧化剂与还原剂的物质的量比是_______;如果反应生成0.3mol的单质碘,则转移的电子数目是_______。
②先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,这时候,观察到的现象是_____;
③若采用下图实验装置将四氯化碳和I2的混合溶液分离。
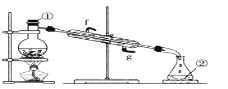
写出图中仪器的名称:①_____;该装置还缺少的仪器是_____;冷凝管的进水口是:_____(填g或f)。
(2)实验室常用MnO2和浓盐酸制氯气,反应原理:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①实验室用MnO2和浓盐酸制氯气的离子方程式:__________________________
②上述反应中氧化剂:__________,还原剂:__________,被氧化的HCl和未被氧化的HCl的比值______________。
③a : Cl2+2I-=I2+2Cl-; b: Cl2+2Fe2+=2Fe3++Cl-; c:2Fe3++2I-=I2+2Fe2+。 Cl2、I2、Fe3+的氧化性由强到弱的顺序:_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
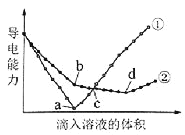
下列分析不正确的是( )
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH–
C.c点,两溶液中含有相同量的OH–
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列实验装置及药品能实现相应实验目的的是

A. 甲用于制取NaHCO3晶体 B. 乙用于分离I2和NH4Cl
C. 丙用于证明非金属性强弱:Cl>C>Si D. 丁用于测定某稀醋酸的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化反应与还原反应在同一元素间进行的是
A.Cl2 + 2NaOH = NaCl + NaClO + H2O
B.Fe + CuSO4 = FeSO4 + Cu
C.2KClO3 ![]() 2KCl + 3O2↑
2KCl + 3O2↑
D.2H2O ![]() 2H2↑+ O2↑
2H2↑+ O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com