
【题目】煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1
2CO(g)+O2(g)===2CO2(g) ΔH2
2H2(g)+O2(g)===2H2O(g) ΔH3
则反应CO(g)+2H2(g)===CH3OH(g)的ΔH=______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。

①T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
②由CO合成甲醇时,CO在250 ℃、300 ℃、350 ℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为________ ℃。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是____________。

③以下有关该反应的说法正确的是________(填序号)。
A.恒温、恒容条件下,若容器内的压强不再发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2 mol CO和6 mol H2充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(3)一定温度下,向2 L固定体积的密闭容器中加入1 mol CH3OH(g),发生反应:CH3OH(g) ![]() CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。

0~2 min内的平均反应速率v(CH3OH)=__________。该温度下,反应CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g)
CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g) ![]() CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
【答案】 ΔH1+![]() ΔH2-
ΔH2-![]() ΔH3 > 350 1.3×104 kPa下CO的转化率已经很高,如果增大压强,CO的转化率提高不大,而生产成本增加很多,得不偿失 AD 0.125 mol·L-1·min-1 4 向正反应方向
ΔH3 > 350 1.3×104 kPa下CO的转化率已经很高,如果增大压强,CO的转化率提高不大,而生产成本增加很多,得不偿失 AD 0.125 mol·L-1·min-1 4 向正反应方向
【解析】(1).已知:①.CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1 ②.2CO(g)+O2(g)===2CO2(g) ΔH2 ③.2H2(g)+O2(g)===2H2O(g) ΔH3
根据盖斯定律,①+②÷2-③÷2得:CO(g)+2H2(g)===CH3OH(g),则△H=ΔH1+![]() ΔH2-
ΔH2-![]() ΔH3,故答案为:ΔH1+
ΔH3,故答案为:ΔH1+![]() ΔH2-
ΔH2-![]() ΔH3;
ΔH3;
(2). ①. 由图象可知,根据“先拐先平数值大”的原则,温度T1<T2,升高温度CO的转化率降低,说明正反应为放热反应,平衡逆向移动,则K值减小,即K1>K2,故答案为:>;
②. 根据上述分析可知,该反应为放热反应,升高温度CO的转化率降低,由图象可知,曲线c对应的CO转化率最低,温度应最高,即为350℃;根据CO在不同温度下的平衡转化率与压强的关系图可知在1.3×104kPa下,CO的转化率已经很高,如果增加压强,CO的转化率提高不大,而生产成本增加,得不偿失,故答案为:350;1.3×104kPa下CO的转化率已经很高,如果增大压强,CO的转化率提高不大,而生产成本增加很多,得不偿失;
③. A. 反应前后气体的物质的量不等,恒温、恒容条件下,若容器内的压强不发生变化,可说明可逆反应达到平衡,故A正确;B. 无论是否达到平衡状态,都存在H2的消耗速率是CO的消耗速率的2倍,因此不能判断是否达到平衡状态,故B错误;C. 使用合适的催化剂能缩短达到平衡的时间,但不能使平衡发生移动,故C错误;D. 某温度下,将2molCO和6molH2充入2L密闭容器中,充分反应达到平衡后,测得c(CO)=0.2mol/L,则剩余0.4molCO,所以CO的转化率为(2mol0.4mol)÷2mol×100%=80%,故D正确;故答案为:AD;
(3).平衡时氢气的浓度为0.5mol/L,则v(H2)=0.5mol/L÷2min=0.25molL1min1,则v(CH3OH)=0.125molL1min1;
CH3OH(g)CO(g)+2H2(g)
起始浓度(mol/L) 0.5 0 0
转化浓度(mol/L) 0.25 0.25 0.5
平衡浓度(mol/L) 0.25 0.25 0.5
则K1=![]() =0.25,求得该反应的化学平衡常数为0.25(mol/L)2,CO(g)+2H2(g)CH3OH(g)是该反应的逆反应,所以K=
=0.25,求得该反应的化学平衡常数为0.25(mol/L)2,CO(g)+2H2(g)CH3OH(g)是该反应的逆反应,所以K=![]() =
=![]() =4;
=4;
某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时Qc=![]() =3<K=4,则平衡向正反应向移动;故答案为: 0.125 mol·L-1·min-1;4;向正反应方向。
=3<K=4,则平衡向正反应向移动;故答案为: 0.125 mol·L-1·min-1;4;向正反应方向。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数.在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便.下列说法不正确的是( )
A.对于C2H4 (g)+H2O(g)?C2H5OH(g),在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为2 mol,则用分压表示的平衡常数Kp= ![]()
B.恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)?2NH3(g)达到平衡状态时,N2、H2、NH3各1mol,若此时再充入3mol N2 , 则平衡正向移动
C.恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)?2C(g)达到平衡时,A、B和 C的物质的量分别为4mol、2mol和4mol,若此时A、B和C均减少1 mol,平衡逆向移动
D.对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为 , 原子个数比为 .
(2)等温等压下,等体积的O2和O3所含分子个数比为 , 原子个数比为 , 质量比为 .
(3)设NA为阿伏伽德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是(用含NA的式子表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气在298 K、100 kPa时,在1 L水中可溶解0.090 mol,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
(1)该反应的离子方程式为______________________________________;
(2)在上述平衡体系中加入少量NaCl固体,平衡将向________移动(填“正反应方向”、“逆反应方向”或“不”)。
(3)如果增大氯气的压强,氯气在水中的溶解度将________(填“增大”、“减小”或“不变”),平衡将向________移动。(填“正反应方向”、“逆反应方向”或“不”)
(4)在饱和氯水中加入石灰石可得到较大浓度的次氯酸溶液,请运用学过的化学原理进行解释(酸性:盐酸>碳酸>次氯酸):_______________________;写出氯水与石灰石反应的离子方程式:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:NaHCO3+H2 ![]() HCOONa+H2O下列有关说法正确的是( )
HCOONa+H2O下列有关说法正确的是( )
A.储氢、释氢过程均无能量变化
B.释氢过程中,每消耗0.1molH2O放出2.24L的H2
C.上述储氢原理和钢瓶储氢原理相同
D.NaHCO3含有离子键和共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.加入苯酚显紫色的溶液:K+、NH4+、Cl﹣、I﹣;加入酚酞呈红色的溶液:SO42﹣、K+、Cl﹣、HSO3﹣分别都不能大量共存(常温下)
B.![]() =1×10﹣12的溶液:K+、AlO2﹣、CO32﹣、Na+; pH=2的溶液:NO3﹣、Fe2+、Na+、Al3+分别都可以大量共存(常温下)
=1×10﹣12的溶液:K+、AlO2﹣、CO32﹣、Na+; pH=2的溶液:NO3﹣、Fe2+、Na+、Al3+分别都可以大量共存(常温下)
C.已知:25℃时,Mg(OH)2的Ksp=5.61×10﹣12 , MgF2的KSP=7.42×10﹣11 , 25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2 可以转化为MgF2
D.表示H2燃烧热的化学方程式为:H2(g)+ ![]() O2(g)═H2O(1);△H=﹣285.8kJ/mol
O2(g)═H2O(1);△H=﹣285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用.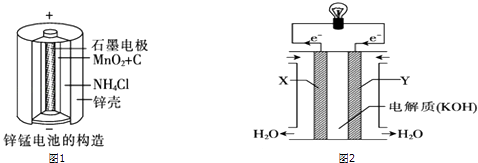
(1)锌锰干电池是应用最普遍的电池之一(如图1所示),锌锰干电池的负极材料是 , 负极发生的电极反应方程式为: . 若反应消耗32.5g 负极材料,则电池中转移电子的数目为 .
(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O ![]() 2Ni(OH)2+Cd(OH)2 , 已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是 . ①以上反应是可逆反应 ②以上反应不是可逆反应
2Ni(OH)2+Cd(OH)2 , 已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是 . ①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
A.①③
B.②④
C.①④
D.②③
(3)图2为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH.则X极为电池的(填“正”或“负”)极,X极的电极反应方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学实验安全问题的叙述中不正确的是
A.少量的浓硫酸沾到皮肤上时,可以直接用大量的水冲洗
B.取用化学药品时,应特别注意观察药品包装上的安全警示标记
C.凡是给玻璃仪器加热时,都要加垫石棉网,以防仪器炸裂
D.闻任何化学药品的气味都不能使鼻子凑近药品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com