
【题目】![]() 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,![]() 无水乙醇所含碳氢键数目为
无水乙醇所含碳氢键数目为![]()
B.足量![]() 与含
与含![]() 的浓盐酸完全反应,转移电子数为
的浓盐酸完全反应,转移电子数为![]()
C.标准状况下,![]() 氦气和氖气的混合气体中原子数为
氦气和氖气的混合气体中原子数为![]()
D.含![]() 和
和![]() 共
共![]() 的
的![]() 溶液中含有的
溶液中含有的![]() 数目为
数目为![]()
科目:高中化学 来源: 题型:
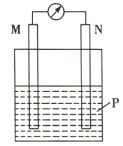
【题目】在如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,其中P为电解质溶液。由此判断M、N、P所代表的物质可能是( )
选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸 |
B | 铜 | 锌 | 稀硫酸 |
C | 银 | 锌 | AgNO3溶液 |
D | 铜 | 铁 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+N(g)![]() E(g),当反应进行到4min时达到平衡,测得M的浓度为0.2mol·L-1。下列说法正确的是( )
E(g),当反应进行到4min时达到平衡,测得M的浓度为0.2mol·L-1。下列说法正确的是( )
A.2min时,M的物质的量浓度为0.6mol·L-1
B.0~4min内,v(M)=0.8mol·L-1·min-1
C.4min后,向容器中充入不参与反应的稀有气体,M的物质的量减小
D.4min时,M的转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案设计及结论均正确的是( )
A.淀粉溶液![]() 水解液
水解液![]() 为蓝。结论:淀粉完全没有水解
为蓝。结论:淀粉完全没有水解
B.淀粉溶液![]() 水解液
水解液![]() 无砖红色沉淀。结论:淀粉完全水解
无砖红色沉淀。结论:淀粉完全水解
C.淀粉溶液![]() 水解液
水解液![]() 中和液
中和液![]() 有砖红色沉淀。结论:淀粉已水解
有砖红色沉淀。结论:淀粉已水解
D.淀粉溶液![]() 水解液
水解液![]() 无现象。结论:淀粉没有水解
无现象。结论:淀粉没有水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图的实验装置可用于研究SO2转化为SO3的转化率。已知:SO3的熔点是16.8℃,沸点是44.8℃。A处为SO2气体发生装置,C处为SO2与O2反应的装置。
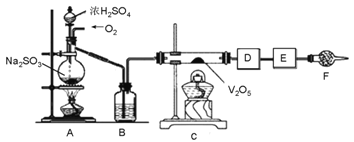
完成下列填空:
(1).A处的化学反应方程式为__________________,仪器F的名称为___________________________。
(2).根据实验需要,应该在D、E处连接合适的装置。请从下图中选择,将所选装置的序号填入相应的空格,D:________________,E:______________。

(3).用amolNa2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间O2,最后测得E处装置增重bg,则此时SO2的转化率为_____%(用含a、b的代数式表示)。
(4).若Na2SO3变质,会影响到SO2的转化。现欲检验某Na2SO3样品是否变质,你的方法是____________________________________________________________________________________________。
(5).实验结束后,如果将收集了SO3的装置敞口露置于空气中,可看到装置出口处产生大量白雾,其原因是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置,用过量浓硫酸与铜反应制取SO2,并探究SO2与Na2O2反应的产物。

Ⅰ.制取SO2
(1)写出烧瓶中生成SO2的化学方程式:_______________________。
(2)写出实验现象:
①细铜丝表面:_______________________________________。
②实验过程中,烧瓶内液体始终保持澄清,并_______________________________。
(3)欲使反应停止,应进行的操作是:______________________________________。
烧瓶中液体冷却后,可观察到的现象是:___________________________________。
Ⅱ.探究SO2与Na2O2反应后的固体产物。
(4)实验方案如下:取洗涤玻璃棉所得溶液,________________________________
(5)把Na2O2粉末散附在玻璃棉上的目的是:__________________________________。
若Na2O2未完全反应,对实验结果的影响是(用必要的文字和化学方程式表示)_______________________________________________________________________
III.装置改进
(6)老师指出该实验装置需做如下改进(只答出一种即可):
___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,可逆反应:A2(g)+ B2(g)![]() xC(g) 符合下列图Ⅰ所示关系,由此推断对图Ⅱ的正确说法是
xC(g) 符合下列图Ⅰ所示关系,由此推断对图Ⅱ的正确说法是
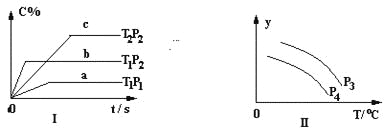
A. P3<P4,Y轴表示A2的转化率
B. P3<P4,Y轴表示A2的浓度
C. P3>P4,Y轴表示混合气体的密度
D. P3>P4,Y轴表示混合气体的平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
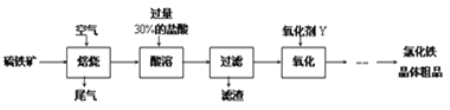
请按要求回答下列问题:
(1)需将硫铁矿粉碎再焙烧的目的是______________________________________.
(2)酸溶及后续过程中均需保持盐酸过量,其目的是_____________、__________.
(3)尾气主要含N2、O2、SO2和少量的CO2、H2O(g).测定尾气中SO2含量的方案如下:
(方案甲)将标准状况下的2.24 L尾气缓慢通过如下装置A中:
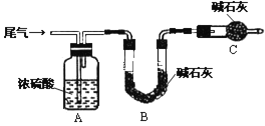
①C仪器的名称是_______________,装置C的作用是_________________________.
②实验时先通入尾气,再通入一定量氮气,通过B装置的增重来测量SO2的体积分数,请写出该方案合理与否的理由__________________________________________.
(方案乙)将标准状况下的2.24 L尾气缓慢通过如下装置D中,充分与足量试剂M反应后,再滴入过量试剂N,经过滤、洗涤、干燥、用电子天平称得沉淀质量为0.233g.
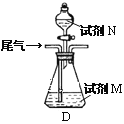
③若试剂M、N分别是碘水、BaCl2溶液,写出D中总反应的离子方程式: __________________.尾气中SO2的体积分数为__________________.
④若试剂M是Ba(NO3)2溶液,不再滴加试剂N,观察到D中生成的无色气体在瓶口处变为红棕色.写出SO2和Ba(NO3)2溶液反应的离子方程式:___________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。下列说法错误的是
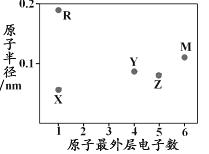
A. R的氧化物含有离子键 B. 最高价含氧酸的酸性:Z<Y
C. M的氢化物常温常压下为气体 D. Y形成的化合物种类最多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com