
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。采用的实验方案如下:
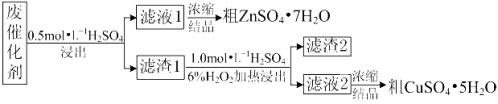
已知:① ZnS与稀硫酸反应时,化合价不变;
② CuS既不溶解于稀硫酸,也不与稀硫酸反应。
回答下列问题:
(1)在下列装置中,第一次浸出必须用________________,第二次浸出应选用______________。(填标号)。第二次浸出时,加热温度不宜过高的原因是 。

(2)滤液1中含有Fe2+,请根据提供的试剂进行检验,则检验方法为: 。
(提供的试剂:稀盐酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水)
(3)将滤液1、滤液2蒸发浓缩至 时,停止加热,然后冷却结晶得到相应的粗产品。
(4)若滤渣2中含有淡黄色固体,写出第二次浸出的化学反应方程式: 。
(5)某同学在实验完成之后,得到1.50 g CuSO4·5H2O,则铜的回收率为___________________。
【答案】(1)D(1分) A(1分) 温度过高H2O2易分解(1分)
(2)取少量滤液1,滴加高锰酸钾溶液,若褪色,则证明有Fe2+。(2分)
(3)溶液表面出现一层晶膜(1分)
(4)CuS+ H2O2+ H2SO4= ![]() CuSO4 +S+ 2H2O(2分)
CuSO4 +S+ 2H2O(2分)
(5)30.0%(2分)
【解析】
试题分析:(1)根据题目化学工艺流程知,第一次浸出发生反应ZnO+H2SO4=ZnSO4+H2O、ZnS+H2SO4=ZnSO4+H2S↑,Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O,有有毒气体生成,必须用氢氧化钠溶液进行尾气处理,选D装置,第二次浸出时发生反应:CuS++H2O2+ H2SO4=CuSO4+S+2H2O,不产生有毒气体,可以选用A装置;温度过高H2O2易分解,所以加热温度不宜过高。
(2)滤液1中含有Fe3+、Fe2+,加入的试剂只能与Fe2+反应,所以检验滤液1中含有Fe2+方法为取少量滤液1,滴加高锰酸钾溶液,若褪色,则证明有Fe2+。
(3)由电解质溶液获得结晶水合物的方法为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,则将滤液1、滤液2蒸发浓缩至溶液表面出现一层晶膜时,停止加热,然后冷却结晶得到相应的粗产品。
(4)废催化剂中加入稀硫酸,SiO2和CuS与稀硫酸不反应,所以滤渣1中有SiO2和CuS,淡黄色固体是硫,所以CuS与H2O2和硫酸反应生成硫酸铜、S和水,反应的化学方程式为CuS+ H2O2+ H2SO4= ![]() CuSO4 +S+ 2H2O。
CuSO4 +S+ 2H2O。
(5)废催化剂中Cu的物质的量为15.0g×12.8%÷96g/mol=0.02mol,1.5g CuSO45H2O中Cu的物质含量的为1.5g÷250g/mol=0.006mol,则铜的回收率为0.006mol÷0.02mol×100%=30%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】两种金属混合物粉末15g,与足量的盐酸反应时生成标准状况下11.2L氢气,符合上述情况的金属混合物是
A.Zn、Fe B.Zn、Ag C.Al、Cu D.Mg、Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物学家借助新的显微技术,成功观察到小于200纳米的粒子.下列分散系中,分散质粒子半径最小的是
( )
A.雾
B.墨水
C.石灰乳
D.KCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)已知氯水有漂白性,是因为含有 (化学式),能与AgNO3反应生成 色沉淀,是因为含有 (名称)离子;
(Ⅱ)在下图所示的物质转化关系中,A是常见的气态氢化物,其水溶液呈碱性,B是能使带火星的木条复燃的无色无味气体, G是一种红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)
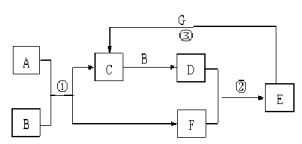
请回答下列问题:
(1)实验室制取A的化学方程式
(2)反应①的化学方程式为 。当有1molA参加反应时,转移 mol电子。
(3)反应②的化学方程式为 。
(4)反应③的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院南京土壤研究所专家通过3年探索土壤中,初步揭开了“长寿之乡”如皋 “寿星”多的秘密:与当地土壤中硒含量息息相关。科研人员发现,当地百岁老人的血液中硒含量比正常人高3倍。硒有抗衰老的作用。这里的“硒”应理解为( )
A. 元素 B. 原子 C. 分子 D. 离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是你,化学是我,化学深入我们生活,下列说法正确的是( )
A. 木材纤维和土豆淀粉遇碘水均显蓝色
B. 食用花生油和鸡蛋清都能发生水解反应
C. 包装用材料聚乙烯和聚氯乙烯都属于烃
D. PX项目的主要产品对二甲苯属于饱和烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00 mL 0.1000 mol·Lˉ1的(NH4)2SO4溶液中逐滴加入0.2000 mol·Lˉ1的NaOH溶液,溶液的pH随NaOH溶液体积的变化如右图所示。下列说法正确的是
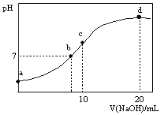
A.点a所示溶液中:c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.点b所示溶液中:c(![]() )=c(Na+)>c(H+)=c(OH-)
)=c(Na+)>c(H+)=c(OH-)
C.点c所示溶液中:c(![]() )+c(H+)=c(NH3·H2O)+c(OH-)
)+c(H+)=c(NH3·H2O)+c(OH-)
D.点d以后的溶液中可能出现:c(![]() )>c(NH3·H2O)>c(OH-)>c(
)>c(NH3·H2O)>c(OH-)>c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图表示的是往某Na2CO3溶液中滴入稀盐酸产生CO2气体的过程。
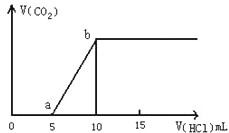
(1)写出a点以前发生反应的离子方程式: 。
(2)写出a点到b点发生反应的离子方程式: 。
(3)若某Na2CO3溶液中含m mol Na2CO3,向其中滴入一定量的稀盐酸,恰好使溶液中Cl-和HCO3-的物质的量之比为2:1,则滴入稀盐酸的物质的量等于 mol(用m表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com