
【题目】关于铝热反应2Al+Fe2O3→2Fe+Al2O3的说法正确的是
A. Al发生氧化反应B. Fe2O3被氧化
C. Fe是还原剂D. Al2O3是还原产物
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】一定条件下乙烯和溴水反应可以得到多种产物,各物质的转化关系如下图.

已知:E的结构简式为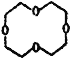 ,I的分子式为C4H4O4,是一种环状化合物。
,I的分子式为C4H4O4,是一种环状化合物。
请回答下列问题:
(1)E的分子式是__ ;B的结构简式是_________。
(2)在乙烯的同系物中,所有碳原子一定共平面且碳原子数最多的分子的结构简式是____,名称是________。
(3)在反应①~⑩中,属于取代反应的是⑥和_____(填写编号);
(4)写出反应⑩的化学方程式___________________。
(5)J是I的同分异构体,且1molJ与足量的NaHCO3溶液反应可放出2molCO2气体,请写出符合条件的J的所有的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中加入氯化钡溶液生成白色沉淀,再加稀盐酸,沉淀不溶解,则该溶液中
A. 一定含SO42―B. 可能含有CO32―和SO42―
C. 一定含有Ag+D. 可能含有SO42―或Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2000 年,德国Freiburg大学的H.Prinzbach宣称,他们通过摘除法,已经在气相质谱仪的气体中发现了最小的球碳分子(富勒烯)——C20(如图所示)。然后在电子冲击质谱仪中观察到了微量C20+和C202+的存在。 他将C20H20 溶解在液溴里,在烧瓶里加压长时间回流,最终得到平均组成为 C20HBr13的产物。

(1)C20的空间构型是正_____面体,其中 C-C σ键数是____, 键角是_______;
(2)C202+中存在的π键数是______;
(3)C20H20分子中 C 原子杂化类型是____杂化, H-C-C 键角比 C-C-C 键角_____(填“大”、“小”或“相等”), C20H20中 C-C σ键长比 C20中______(填“长”、“短” 或“相等”);
(4)如果我们将C20HBr13看成唯一的有机产物,请配平下列方程式:
C20H20+Br2 ![]() C20HBr13+________ 。
C20HBr13+________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化锌荧光材料的研究从1868年法国化学家Sidot发现至今已有近150年的历史。其中立方硫化锌的晶胞如图所示。请回答下列问题:

(1)锌元素在周期表中的位于第______周期_____族, 属于_____区;
(2)基态锌原子的价电子排布式为_________;
(3)一般锌元素常表现为+2 价的原因是_____;
(4)立方硫化锌晶体的每个晶胞中含有_____个锌离子, 其配位数为_____;含有_____个硫离子,其配位数为_____;
(5)根据神奇的“百度”显示,该晶胞的棱长a=541pm,S2-的半径约为184pm,则 Zn2+在此晶胞中的半径大约为______pm(精确到1pm)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是短周期的五种元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可两两反应;A与C同主族;B与E同主族;E的单质为淡黄色晶体,易溶于二硫化碳。
(1)画出C元素的离子结构示意图____________________
(2)写出C、D的最高价氧化物对应水化物相互反应的离子方程式________________
(3)B、C、D、E四种元素的原子半径由大到小的排列顺序为(用元素符号表示)
______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A、B、C、D、E、F有以下转化关系.A的产量是衡量一个国家石油化工生产水平的标志;D能使石蕊试液变红;E是不溶于水且具有水果香味的无色液体,相对分子质量是C的2倍;F是塑料的主要成分之一,常用于制食品包装袋.结合如图关系回答问题:

(1)按要求回答下列问题:
①写出A、E的结构简式:A______、E______;
②写出B、C、D、E中官能团的名称:B______、C、______D______E、______;
③写出反应②的反应方程式:_______________________________________
(2)A与苯都是石油化工的重要产品,在一定条件下A可以转化生成苯,按要求回答下列问题:
苯可以发生取代反应,写出由苯制备溴苯的化学反应方程式:________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.利用CO2和CH4重整可制合成气(主要成分为CO、H2),已知重整过程中部分反应的热化学方程式为:
① CH4(g) = C(s)+2H2(g) △H= + 75.0 kJ·mol—1
② CO2(g)+H2(g)= CO(g)+H2O(g) △H = + 41.0 kJ·mol—1
③ CO(g)+H2(g) = C(s)+H2O(g) △H = -131.0 kJ·mol—1
反应CO2(g)+CH4(g) = 2CO(g)+2H2(g)的△H =___________kJ·mol—1。
II.用CO合成尿素的反应为:2NH3(g) + CO(g)![]() CO(NH2)2(g) + H2(g) ΔH <0。
CO(NH2)2(g) + H2(g) ΔH <0。
(1)T ℃时,向体积为2 L的恒容密闭容器中,充入2 molNH3和1 mol CO发生反应。
① 5 min时反应达到平衡状态,CO的转化率为80%,则5 min内NH3的平均反应速率为________,此温度下反应的平衡常数K的值为 ____________ 。
②对该反应,下列说法正确的是______(填字母)。
A.若容器内气体密度不变,则表明反应达到平衡状态
B.反应达到平衡后,其它条件不变,升高温度,尿素的百分含量增大
C.反应达到平衡后,其它条件不变,在原容器中充入一定量氦气,CO的转化率不变
D.反应达到平衡后,其它条件不变,充入一定量NH3,平衡向正反应方向移动,但K值不变
(2)若保持恒温恒容条件,将物质的量之和为3 mol的NH3和CO以不同的氨碳比进行反应,结果如图所示:若图中c表示平衡体系中尿素的体积分数,则b表示________的转化率。当尿素含量最大时,则![]() =______,此时,对于该反应既能增大反应速率又能提高尿素体积分数的措施为_____。
=______,此时,对于该反应既能增大反应速率又能提高尿素体积分数的措施为_____。

Ⅲ.下图是铬酸银(Ag2CrO4)T ℃时,在水溶液中的沉淀溶解平衡曲线。

(1)向饱和Ag2CrO4溶液中加入固体K2CrO4______(填“能”或“不能”)使溶液由Y点变为X点
(2)图中ɑ = _________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com