
| A. | AgCl在饱和NaCl溶液中的 KSP 比在纯水中的 KSP 小 | |
| B. | 向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP (AgCl)<KSP (AgBr) | |
| C. | 将0.001 mol•L- 1 的AgNO3 溶液滴入0.001 mol•L- 1 的KCl和0.001 mol•L- 1 的K2CrO4 溶液中先产生Ag2CrO4 沉淀 | |
| D. | 向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
分析 A.KSP只于温度有关;
B.沉淀转化为溶解度更小的物质容易发生;
C.Qc与KSP差别越大,越容易生成沉淀;
D.银离子与氨水生成氢氧化二氨合银.
解答 解:A.KSP只于温度有关,与溶液中离子浓度无关.故A错误;
B.沉淀转化为溶解度更小的物质容易发生,向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP(AgCl)>KSP(AgBr).故B错误;
C.在AgCl饱和溶液中,Qc(AgCl)=c(Ag+)•c(Cl-)=0.001mol•L-1×0.001mol•L-1=1×10-6mol2•L-2>1.8×10-10mol2•L-2,在Ag2CrO4饱和溶液中,Qc(Ag2CrO4)=c(Ag+)2•c(CrO42-)=0.001mol•L-1×0.001mol•L-1×0.001mol•L-1=1×10-9mol3•L-3>1.9×10-12mol3•L-3,所以均会产生沉淀,但以AgCl沉淀为主在AgCl饱和溶液中,故C错误;
D.银离子与氨水生成氢氧化二氨合银,使平衡向右移动.故D正确.
故选D.
点评 本题考查难溶电解质的溶解平衡及沉淀转化的本质,为高频考点,侧重于学生的分析能力的考查,注意沉淀转化为溶解度更小的物质容易发生,难度不大.


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 焰色反应 | B. | 氧化性 | C. | 还原性 | D. | 不稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | NaHCO3的电离方程式:NaHCO3?Na++HCO3- | |
| C. | Fe 与盐酸反应制 H2:2Fe+6H+═2Fe3++3H2↑ | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ),是常用的解热镇痛药,实验室合成流程如下:
),是常用的解热镇痛药,实验室合成流程如下:

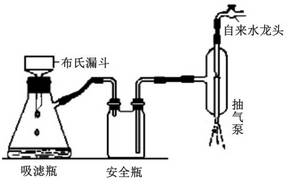
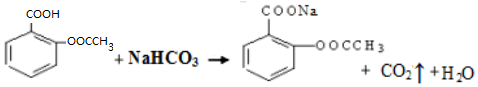 .
.

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(SO3)/mol | n(O2)/mol |
| 0 | 2.0 | 0 |
| 2 | 0.8 | |
| 4 | 0.6 | |
| 6 | 1.8 | 1.1 |
| A. | 0~2 min平均速率v(SO2)=0.6 mol•L-1•min-1 | |
| B. | 4 min后,平衡移动的原因可能是减压 | |
| C. | 若升高温度后的平衡常数的值为1.0,则该正反应为吸热反应 | |
| D. | 若起始时容器中SO3的物质的量改为1.0 mol,则平衡时n(SO2)=0.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
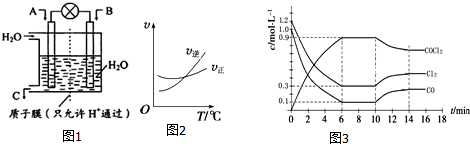
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 低温、低压 | B. | 低温、高压 | C. | 高温、高压 | D. | 高温、低压 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com