
【题目】某研究小组为了探究一种抗酸药X(仅含五种短周期元素)的组成和性质,设计并完成了如下实验:
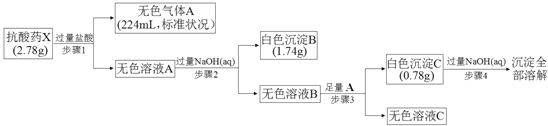
请回答下列问题:
(1)白色沉淀B中金属元素的离子结构示意图为_______,A的电子式为__________.
(2)步骤3中生成沉淀C的离子方程式为______________________________.
(3)X的化学式为______________,该抗酸药不适合胃溃疡重症患者使用,原因是______________________________.
(4)设计实验方案验证溶液C中的含碳酸氢根离子____________________________.
【答案】 )
![]() AlO2﹣+CO2+2H2O=Al(OH)3↓+HCO3﹣ AlMg3(CO3)(OH)7 和胃酸反应生成二氧化碳容易造成胃穿孔 取少量溶液C,先滴入BaCl2溶液,无明显现象,再滴入NaOH溶液,有白色沉淀产生,则溶液C中含有碳酸氢根离子
AlO2﹣+CO2+2H2O=Al(OH)3↓+HCO3﹣ AlMg3(CO3)(OH)7 和胃酸反应生成二氧化碳容易造成胃穿孔 取少量溶液C,先滴入BaCl2溶液,无明显现象,再滴入NaOH溶液,有白色沉淀产生,则溶液C中含有碳酸氢根离子
【解析】根据题给流程和信息确定气体A为CO2,沉淀B为氢氧化镁,沉淀C为氢氧化铝。(1)白色沉淀B为氢氧化镁,镁离子的离子结构示意图为 ,A为二氧化碳,电子式为
,A为二氧化碳,电子式为![]() ;
;
(2)根据题给流程判断无色溶液中含有AlO2﹣,向其中通入足量二氧化碳生成氢氧化铝沉淀和碳酸氢根,离子方程式为AlO2﹣+CO2+2H2O=Al(OH)3↓+HCO3﹣;(3)二氧化碳在标准状况下的体积为224mL,物质的量为0.01mol,则X中含碳酸根的物质的量为0.01mol,质量为0.6g;m[Mg(OH)2]=1.74g,则X中含Mg2+的物质的量为:n(Mg2+)= n[Mg(OH)2]=0.03mol,m(Mg2+)=0.72g;m[Al(OH)3]=0.78g,则X中含Al3+的物质的量为:n(Al3+)= n[Al(OH)3]=0.01mol,m(Al3+)=0.27g;又X为抗酸药,则其中含氢氧根,质量为(2.78-0.6-0.72-0.27)g=1.19g,物质的量为0.07mol,则X的化学式为Mg3Al(OH)7CO3或[2Mg(OH)2·Al(OH)3·MgCO3],该抗酸药不适合胃溃疡重症患者使用,原因是该抗酸药与胃酸反应生成CO2,可能导致胃穿孔;(4)验证步骤3后得到的无色溶液C中含有碳酸氢根离子的实验方案为:取少量溶液C,先滴入BaCl2溶液,无明显现象,再滴入NaOH溶液,有白色沉淀产生,则溶液C中含有HCO3-。


科目:高中化学 来源: 题型:
【题目】A~G各物质间的关系如图,其中B为可使带火星木条复燃的气态单质、D为黄绿色气态单质。
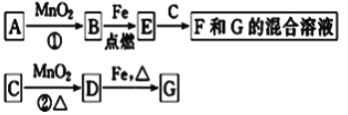
请回答下列问题:
(1)物质B和D分别为__________________________
(2)MnO2在反应①和②中的作用分别是______________________________
(3)新配制的F溶液应加入_____以防止其转化为G.检验G溶液中阳离子的常用试剂是________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白原理相同
②向100mL0.1mol/L 的溴化亚铁溶液中通入0.05mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2=2 Fe3++2Br2+6Cl-
③电解精炼铜时,以粗铜作阴极,纯铜作阳极
④钢铁的吸氧腐蚀负极电极反应式 :Fe-3e-=Fe3+
⑤碳酸氢根离子的电离方程式可表示为: HCO3- + H2O![]() H3O++ CO32-
H3O++ CO32-
⑥SiO2 虽是酸性氧化物,但其不溶于水,因此不能与NaOH溶液反应
⑦ CO、SO2、NO、NO2都是对大气产生污染的气体,他们在空气中都能稳定存在
⑧浓硫酸具有脱水性,所以可以做干燥剂
A.②④⑧ B.②⑤ C.③④⑥ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaHCO3和Na2CO3·10H2O混和物6.56g溶于水制成100mL溶液,测得溶液中c(Na+)=0.5mol/L。向该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量为
A. 2.93 g B. 5.85 g C. 6.56g D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号中注明的方法分离下列各组混合物,其中不正确的是( )
A. 汽油和煤油(蒸馏) B. 食盐中的沙子(溶解过滤)
C. 氯化钠和水(过滤) D. 花生油和水(分液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙二醇是重要的化工原料,利用甘油制备二元醇符合绿色化学要求.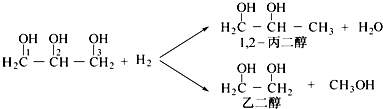
利用1,2﹣丙二醇可制得乳酸〔CH3CH(OH)COOH〕,乳酸与上述反应中的某一产物B可以反应,转换关系如下.已知A的碳原子数与乳酸相同,E、F为链状高分子化合物.请回答下列问题: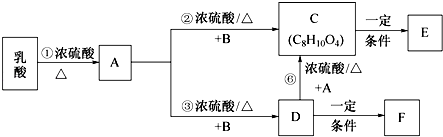
(1)反应①的反应类型是反应,A中所含官能团名称是 .
(2)B在一定条件下反应生成分子式为C2H4O的有机物,该物质不能发生银镜反应,核磁共振氢谱中只有一个峰,写出该物质的结构简式 .
(3)F具有良好的光学性能和亲水性可作为隐形眼镜的材料,写出由D制备F的化学方程式 .
(4)写出1,2﹣丙二醇制备乳酸的合成路线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数为98%、密度为1.84g/mL的浓硫酸来配制480mL0.2mol/L 的稀硫酸。可供选择的仪器有: ①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙。完成下列问题:
(1)上述仪器中,在配制稀硫酸时不需要用到的是______ (填仪器序号)。
(2)配制过程中需选用的容量瓶规格为_____mL,经过计算,需要量取的浓硫酸体积为_____mL。
(3)在配制过程中,下列操作使所配溶液浓度偏高的是______ (填字母)。
a.未洗涤稀释浓硫酸所用的烧杯和玻璃棒
b.为防止变质,稀释后的硫酸溶液立即就转移到容量瓶中
C.移液前,容量瓶中含有少量蒸馏水
d.定容时,俯视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com