
下述实验不能达到预期实验目的的是( )
| 序号 | 实验内容 | 实验目的 |
| A | 将2.5gCuSO4·5H2O溶解在97.5g水中 | 配制质量分数为1.6%的CuSO4溶液 |
| B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
科目:高中化学 来源: 题型:
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g) CH4(g)+HC≡CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH3CH=CH2(g) CH4(g)+HC≡CH(g) △H2=32.4 kJ·mol-1
CH4(g)+HC≡CH(g) △H2=32.4 kJ·mol-1
则相同条件下,反应C3H3(g) CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1
CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为___________;放电时, 移向电池的_______(填“正”或“负”)极。
移向电池的_______(填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3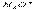
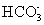 +H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
+H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液c(H2CO3)______c( )(填“>”、“=”或“<”),原因是__________(用离子方程式和必要的文字说明)。
)(填“>”、“=”或“<”),原因是__________(用离子方程式和必要的文字说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
X是核外电子数最少的元素,Y是地壳中含量最多的元素,Z在地壳中的含量仅次于Y,
W可以形成自然界最硬的原子晶体。下列叙述错误的是( )
A.WX4是沼气的主要成分 B.固态X2Y是分子晶体
C.ZW是原子晶体 D.ZY2的水溶液俗称“水玻璃”
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,下列关于C3N4晶体的说法正确的是 ( )
已知C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,下列关于C3N4晶体的说法正确的是 ( )
A.C3N4晶体是分子晶体
B.C3N4晶体中微粒间通过离子键结合
C.C3N4晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子
D.C3N4晶体中, C-N键的键长比金刚石中的C-C键的键长要长
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列溶液中,能大量共存的离子组是( )
A.能使pH试纸显蓝色的溶液中: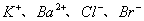
B.常温下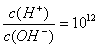 的溶液中:
的溶液中: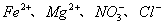
C.含有大量Al3+的溶液中: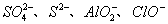
D.常温下pH为7的溶液中: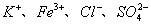
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂溶解在亚硫酰氯(SOCl2)中形成,电池的总反应式为8Li+3SOCl2=6LiCl+Li2SO3+2S,则下列叙述正确的是 ( )
A.用该电池电解CuCl2溶液产生2.24LCl2时,有0.2mol电子转移
B.金属锂作电池的负极,石墨作电池的正极,加入硫酸可提高电解质的导电性
C.电池工作(放电)过程中,SOCl2被还原为Li2SO3
D.电池工作过程中,负极消耗的锂与正极生成的硫质量之比为7:8
查看答案和解析>>
科目:高中化学 来源: 题型:
亚铁是血红蛋白重要组成成分,起着向人体组织传送O2的作用,如果缺铁就可能出现缺铁性贫血,但是摄入过量的铁也有害。下面是一种常见补药品说明书中的部分内容:该药品含Fe2+33%~36%,不溶于水但能溶于人体中的胃酸:与Vc(维生素C)同服可增加本品吸收。
(一)甲同学设计了以下下实验检测该补铁药品中是否含有Fe2+并探究Vc的作用:

(1)加入新制氯水后溶液中发生的离子反应方程式是_________________________、
Fe3+ +SCN- [Fe(SCN) ]2+ 。
[Fe(SCN) ]2+ 。
(2)加入KSCN溶液后溶液变为淡红色,说明溶液中有少量Fe3+。该离子存在的原因可能是(填编号)_____________________。
A.药品中的铁本来就应该以三价铁的形式存在
B.在制药过程中生成少量三价铁
C.药品储存过程中有少量三价铁生成
(3)药品说明书中“与Vc同服可增加本品吸收”请说明理由_______________________。
(二)乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为 。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
(4)该实验中的试剂2与甲同学设计的实验中的试剂1都可以是______(填序号)。
A.蒸馏水B.稀盐酸C.稀硫酸D.稀硝酸
(5)本实验滴定过程中操作滴定管的图示正确的是_______(填编号)。

(6)请通过计算,说明该药品含“铁”量是否合格(写出主要计算过程)?
查看答案和解析>>
科目:高中化学 来源: 题型:
将标准状况下的aL HCl(g)溶于1000g水中,得到的盐酸密度为b g·cm-3,则该盐酸的物质的量浓度是 ( )
A.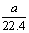 mo1·L-1 B.
mo1·L-1 B.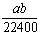 mol·L-1 C.
mol·L-1 C.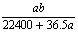 mol·L-1 D.
mol·L-1 D.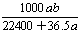 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
|
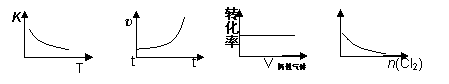
 CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是
CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是 ① ② ③ ④
A.①表示随温度升高,平衡常数的变化
B.②表示加入催化剂,反应速率随时间的变化
C.③表示恒压条件下,反应物的转化率随充入惰性气体体积的变化
D.④表示CO的体积分数随充入Cl2量的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com