
已知反应FeO(s)+CO(g) 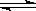 Fe(s)+CO2(g)
的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
Fe(s)+CO2(g)
的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(1)反应正向进行 (2)c(CO)平=0.04mol/L c(CO2)平=0.02mol/L (3)20
【解析】
试题分析:(1)根据平衡常数的表达式可知,如果起始浓度c(CO) = 0.05 mol·L-1,c(CO2)
= 0.01 mol·L-1,则此时K=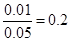 <0.5,所以反应向正反应方向进行。
<0.5,所以反应向正反应方向进行。
(2)设平衡时生成CO2的浓度是x,则根据平衡常数的表达式可知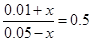 ,解得x=0.01mol/L,则反应物、生成物的平衡浓度分别是0.04mol/L和0.02mol/,其中CO的转化率是
,解得x=0.01mol/L,则反应物、生成物的平衡浓度分别是0.04mol/L和0.02mol/,其中CO的转化率是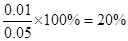 。
。
考点:考查平衡常数的有关计算
点评:该题是中等难度的试题,试题基础性强,侧重对学生基础知识的巩固和训练。该题的关键是明确平衡常数的含义,然后依据方程式灵活运用即可。有利于培养学生的逻辑推理能力,提高学生分析、归纳、总结问题的能力。


科目:高中化学 来源: 题型:
已知反应FeO(s)+CO(g)![]() Fe(s)+CO2(g)的Kc=0.5(1 273 K)。若起始浓度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,请回答:
Fe(s)+CO2(g)的Kc=0.5(1 273 K)。若起始浓度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加FeO的量,对平衡有无影响?
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省杭州市西湖高级中学高二5月月考化学试卷(带解析) 题型:计算题
已知反应FeO(s)+CO(g)  Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应FeO(s)+CO(g) = Fe(s)+CO2(g) 的平衡常数K=0.5(1273K)。若起始浓度c(CO)= 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加的FeO量会不会促使平衡向正方向移动?
查看答案和解析>>
科目:高中化学 来源:河南省郑州四中09-10学年高二下学期第一次调考(2010郑州四中高二调考) 题型:填空题
已知反应FeO(s)+CO(g) = Fe(s)+CO2(g) 的平衡常数K=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加的FeO量会不会促使平衡向正方向移动?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com