
| A、2.4 g金属镁所含电子数目为0.2 NA |
| B、1 mol H2SO4所含粒子数目为NA |
| C、17 g NH3所含中子数目为10 NA |
| D、18 g水所含分子数目为NA |


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
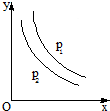 反应:aL(s)+bG(g)?cR(g)达到平衡,温度和压强对该反应的影响如下图所示,图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断( )
反应:aL(s)+bG(g)?cR(g)达到平衡,温度和压强对该反应的影响如下图所示,图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断( )| A、减小压强,混合气体的平均相对分子质量减小 |
| B、上述反应是吸热反应 |
| C、a+b>c |
| D、无法确定a、b的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀有气体的晶体中不存在分子间作用力 |
| B、次氯酸分子的结构式为H-O-Cl |
| C、Na2O和Na2O2所含化学键类型完全相同 |
| D、Br2蒸气被木炭吸附时共价键被破坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A晶体一定是离子晶体 |
| B、若Y的原子序数为m,则X的原子序数只能是m+4或m-4或m-12或m+6或m-2 |
| C、XY3溶于水后可能显酸性或碱性 |
| D、X和Y一定不属于同一主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18gH2O中所含电子数与NA个 NH4+所含电子数相同 |
| B、1 mol Na2O2固体中含离子总数为3NA |
| C、13g锌粒加入浓硫酸,反应后锌粒无剩余,得到标况下气体4.48L |
| D、将饱和食盐水加热蒸发少量水,冷却至原温度,溶液的质量分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、20mL |
| B、30mL |
| C、大于30mL |
| D、大于20mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com