
【题目】一定温度下,将4molPCl3和2molCl2充入容积不变的密闭容器中,在一定条件下反应:PCl3+Cl2PCl5 , 各物质均为气态.达平衡后,PCl5为0.8mol.若此时再移走2molPCl3和1molCl2 , 相同温度下达到平衡,PCl5的物质的量为( )
A.0.8mol
B.0.4mol
C.0.4mol<x<0.8mol
D.<0.4mol
【答案】D
【解析】解:达平衡后移走2.0mol PC13和1.0mol C12 , 重新到达的平衡,可以等效为开始加入2.0mol PC13和1.0molC12到达的平衡,与原平衡相比压强减小,平衡向逆反应移动,反应物的转化率减小,故达新平衡时PC15的物质的量小于原平衡的 ![]() 倍,即达平衡时PC15的物质的量小于0.8mol×
倍,即达平衡时PC15的物质的量小于0.8mol× ![]() =0.4mol,故选D
=0.4mol,故选D
达平衡后移走2.0mol PC13和1.0mol C12 , 重新到达的平衡,可以等效为开始加入2.0mol PC13和1.0mol C12到达的平衡,与原平衡相比压强减小,平衡向逆反应移动,反应物的转化率减小,故平衡时PC15的物质的量小于原平衡的 ![]() 倍.
倍.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知反应N2O4(g) ![]() 2NO2(g) △H>0,平衡体系中总质量
2NO2(g) △H>0,平衡体系中总质量![]() 与总物质的量
与总物质的量![]() 之比M(M=
之比M(M=![]() /
/![]() )在不同温度下随压强变化曲线如图所示。下列说法正确的是:
)在不同温度下随压强变化曲线如图所示。下列说法正确的是:
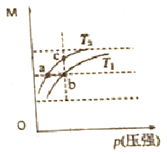
A. 温度:T1 <T2
B. 平衡常数K(a)=K(b)<K(c)
C. 反应速率: ![]()
D. 当M=69g·mol-1 时,n(NO2):n(N2O4)=1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数约为6.02×1023 mol﹣1(NA),下列说法正确的是( )
A.常温常压下,16g O2与16g O3所含的原子数均是NA
B.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl﹣个数为 NA
C.标准状况下,2.24LCCl4所含原子数为0.5NA
D.标准状况下,22.4 L氦气所含有的质子数目约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为教科书中电解饱和食盐水的实验装置.据此,下列叙述不正确的是( ) 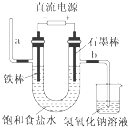
A.装置中,a管能产生氢气
B.在石墨棒电极区域有NaOH产物
C.b管导出的是氯气
D.以食盐水为基础原料制取氯气等产品的工业称为“氯碱工业”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在298K时下述反应的有关数据:
C(s)+ ![]() O2(g)=CO(g)△H1=﹣110.5kJ/mol
O2(g)=CO(g)△H1=﹣110.5kJ/mol
C(s)+O2(g)=CO2(g),△H2=﹣393.5kJ/mol
则C(s)+CO2(g)=2CO(g)的△H 为( )
A.283.5kJ/mol
B.172.5kJ/mol
C.﹣172.5kJ/mol
D.﹣504 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶标签上注明为葡萄糖酸盐的复合剂,可能含有钠、镁、钙、铁等元素.某同学为了确认其中的金属元素,取部分该制剂作为试液,进行如下实验.已知:溶液pH=4时,Fe3+沉淀完全,Ca2+、Mg2+不沉淀.
请回答下列问题:
(1)根据现象1(填“能”或“不能”)确定该试液中含有Na+ .
(2)现象3中白色沉淀的化学式是 .
(3)溶液A中加入H2O2溶液的目的是 .
(4)根据以上实验,可以推断出此葡萄糖酸盐的复合剂中一定含有的元素是 , 一定不含有的元素是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1;
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJmol﹣1 .
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1:1
B.1:3
C.1:4
D.2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有200mLMgCl2和AlCl3的混合溶液,其中c(Mg2+)为0.2mol/L,c(Cl﹣)为1.3mol/L,要使Mg2+与Al3+完全分离,至少需加4mol/L的NaOH溶液的体积为( )
A.40mL
B.72mL
C.80mL
D.128mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com