
【题目】已知在298K时下述反应的有关数据:
C(s)+ ![]() O2(g)=CO(g)△H1=﹣110.5kJ/mol
O2(g)=CO(g)△H1=﹣110.5kJ/mol
C(s)+O2(g)=CO2(g),△H2=﹣393.5kJ/mol
则C(s)+CO2(g)=2CO(g)的△H 为( )
A.283.5kJ/mol
B.172.5kJ/mol
C.﹣172.5kJ/mol
D.﹣504 kJ/mol
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+, Mg2+,SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序
①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液
A. ④②⑤ B. ②⑤④①③ C. ④①②⑤③ D. ①④②⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.1mol/LNaOH溶液480mL,下列叙述正确的是( )
A.需要用托盘天平称量NaOH固体的质量为1.92g
B.将NaOH固体在小烧杯中加水溶解后立即倒入容量瓶中并进行定容
C.在容量瓶中定容时俯视容量瓶刻度线会使溶液浓度偏高
D.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将4molPCl3和2molCl2充入容积不变的密闭容器中,在一定条件下反应:PCl3+Cl2PCl5 , 各物质均为气态.达平衡后,PCl5为0.8mol.若此时再移走2molPCl3和1molCl2 , 相同温度下达到平衡,PCl5的物质的量为( )
A.0.8mol
B.0.4mol
C.0.4mol<x<0.8mol
D.<0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系比较正确的( ) 
A.在A,B间任意一点,溶液中一定都有c(Na+)>cCH3COO﹣)>c(OH﹣)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO﹣)>c(OH﹣)=c(H+)
C.在C点:c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
D.在D点:c(CH3COO﹣)+c(CH3COOH)=2 c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡是无色液体,熔点﹣33℃,沸点114℃.氯气与金属锡在加热时反应可以用来制备SnCl4 , SnCl4极易水解,在潮湿的空气中发烟.实验室可以通过图装置制备少量SnCl4 (夹持装置略). 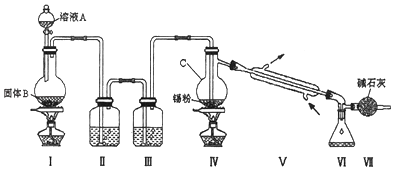
(1)仪器C的名称为:;
(2)装置Ⅰ中发生反应的离子方程式为:;
(3)装置Ⅱ中的最佳试剂为 , 装置Ⅶ的作用为;
(4)若装置连接顺序为Ⅰ﹣Ⅱ一Ⅳ一Ⅴ一Ⅵ一Ⅶ,在Ⅳ中除生成SnCl4外,还会生成的含锡的化合物的化学式为 .
(5)Ⅳ中加热的作用之一是促进氯气与锡粉反应,加热的另一作用为;
(6)若Ⅳ中用去锡粉11.9g,反应后,Ⅵ中锥形瓶里收集到23.8g SnCl4 , 则SnCl4的产率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用钛白工业的副产品FeSO4(含TiO2+、Al3+)可以生产电池级高纯超微细草酸亚铁.其工艺流程如图: 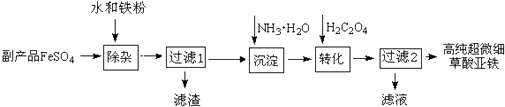
(1)已知过滤1得到的滤渣的主要成分是Al(OH)3、H2TiO3 , 请写出TiOSO4水解成 H2TiO3沉淀的化学方程式:;铁粉的作用有:①除去溶液中的Fe3+ , ② .
(2)沉淀反应的离子方程式是 .
(3)沉淀过程的反应温度为40℃,温度不宜过高的原因除控制沉淀的粒径之外,还有 .
(4)FeC2O4生成时,要在真空环境下进行,原因是 .
(5)过滤2得到的滤液经蒸发浓缩、 , 可得到副产品.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素A、B、C、D、E,原子序数依次增大.A的核外电子总数与其周期数相同,B的价电子层中的未成对电子有3个,C的s能级电子总数与p能级电子总数相等,D与C同族;E的最外层只有1个电子,但次外层有18个电子.回答下列问题:
(1)E+离子的基态核外电子排布
(2)B、C、D中第一电离能由大到小的顺序为(填元素符号)
(3)A和B、C两元素形成的两种共价化合物发生反应,生成BA4+离子,该离子的中心原子的杂化方式为;与BA4+离子互为等电子体的一种分子为(填化学式).
(4)E的硫酸盐溶液中滴加过量的氨水可以生成配合物[E(NH3)4]SO4 , 1mol配合物中含有的σ键的数目为 .
(5)E和C(空心小球为C,实心小球为E)形成的一种离子化合物的晶体结构如图所示,则离子化合物的化学式为 . 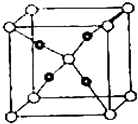
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com