
【题目】工业上,向500℃左右的铁屑中通入Cl2生产无水氯化铁,其制备过程中均要确保无水。现模拟该过程用图示装置进行实验:

(1)仪器a的名称为________,装置A的圆底烧瓶中发生反应的化学方程式为________,为保持装置C为无水环境,装置B中加入的试剂是________。
(2)实验步骤:如图连接装置后,先________(填实验操作),再装药品,然后点燃________(填“A”或“C”)处酒精灯,当________(填实验现象)时,再点燃________(填“A”或“C”)处酒精灯。
(3)装置D的作用是________,________。
(4)甲同学认为进入装置C的气体中混有HCl,应在装置B前增加装有________(填试剂名称)的洗气装置除去;乙同学认为不需要除去HCl,理由为________。
【答案】分液漏斗MnO2+4HCI(浓) ![]() MnCl2+Cl2↑+2H2O浓硫酸检查装置气密性A C中充满黄绿色气体C除去未反应的氯气防止空气中的水蒸气进入C装置饱和食盐水只要氯气足量,最终产物只有氯化铁(合理答案均可得分)
MnCl2+Cl2↑+2H2O浓硫酸检查装置气密性A C中充满黄绿色气体C除去未反应的氯气防止空气中的水蒸气进入C装置饱和食盐水只要氯气足量,最终产物只有氯化铁(合理答案均可得分)
【解析】(1)仪器a的名称为分液漏斗,A装置制取的是氯气,实验室常用浓盐酸与二氧化锰加热制取,化学反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;为保持装置C为无水环境,装置B中加入的试剂是浓硫酸;
MnCl2+Cl2↑+2H2O;为保持装置C为无水环境,装置B中加入的试剂是浓硫酸;
(2)实验中有氯气生成,所以要先检验实验装置的气密性,为排除装置中的空气,应先点燃A处的酒精灯,生成氯气排除空气中的氧气和水蒸气,C中充满黄绿色气体后,再点燃C处酒精灯;
(3)装置D中碱石灰的作用是除去未反应的氯气防止空气中的水蒸气进入C装置;
(4)可用饱和食盐水除去氯气中混有的HCl气体,则应在装置B前增加装有饱和食盐水的洗气装置除去;混有的HCl与Fe生成FeCl2,只要氯气过量,FeCl2会被氯气氧化为FeCl3,不影响产品的纯度。


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】某铁矿石(若只含铁的氧化物和SiO2)取36g溶于过量的稀盐酸中,过滤、洗涤、干燥后得5.6g不溶物,向得到的滤液中加入足量的NaOH溶液,过滤、洗涤后将沉淀灼烧,得32g红棕色固体.根据题意下列结论不正确的是( )
A. 由铁矿石转化为红棕色固体的过程中发生了氧化还原反应
B. 溶于盐酸后得到的滤液中n(Fe2+):n(Fe3+)=1:1
C. 铁矿石中的铁的氧化物的化学式一定是Fe3O4
D. 若稀盐酸为3.0molL﹣1 400mL,反应前后体积变化忽略不计,则滤液中剩余H+的物质的量浓度是0.5molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法或操作中,正确的有( )
①标准状况下,1 mol溴单质的体积约为22.4 L ②用托盘天平称量50.56 g KCl固体 ③用酒精从饱和碘水中萃取碘
④让一束光通过胶体,从垂直于光线的方向可以看到一条光亮的“通路” ⑤从含有少量氯化钠的硝酸钾溶液中提取硝酸钾可用结晶的方法
A. 1个 B. 2个
C. 3个 D. 4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类数相同
B. 乙烷、苯、裂化汽油溶液均不能使酸性高锰酸钾溶液褪色
C. 苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环已烷的密度都比水大
D. 乙酸乙酯在碱性条件下的水解反应称为皂化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
A.2v(NH3)=v(CO2)
B.密闭容器中c(NH3)∶c(CO2)=2∶1
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象不正确的是
A. 向100ml0.1mol·L-1H2SO3溶液中滴加0.1mol·L-1Ba(OH)2溶液至过量
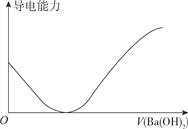
B. 向100ml0.1mol·L-1H2SO4溶液中加入NaOH固体
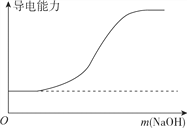
C. 向一定浓度的氯化钠溶液中加水
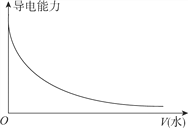
D. 向蒸馏水中通入HCl气体
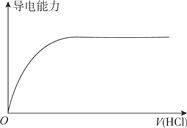
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块镁铝合金投入到20 mL 1 mol/L的HCl溶液里,待合金完全溶解后,往溶液里加入1 mol/L的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积(mL)变化的关系如图所示。下列说法中正确的是( )
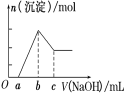
A.镁铝合金具有很强的抗腐蚀能力,它不溶解在任何酸、碱或盐中
B.c值越大,合金中Al的含量越高
C.b值越大,合金中Mg的含量越高
D.假设c=25,整个实验过程中,只发生了4个离子反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下的2L密闭容器,进行反应2X(g)+Y(g) ![]() 2Z(g),若起始时X、Y、Z物质的量分别为n1、n2、n3(均不为零)。达平衡时,X、Y、Z浓度分别为0.2mol/L、0.1 mol /L和0.08 mol/L,则下列判断合理的是( )
2Z(g),若起始时X、Y、Z物质的量分别为n1、n2、n3(均不为零)。达平衡时,X、Y、Z浓度分别为0.2mol/L、0.1 mol /L和0.08 mol/L,则下列判断合理的是( )
A. X和Y的转化率不一定相等
B. n1、n2=2:1
C. 平衡时,Y和Z的生成速率之比为2:1
D. n1的取值范围为0<n1<0.28
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1 mol·L-1醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示。
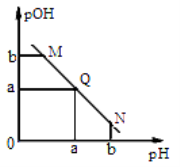
下列说法正确的是( )
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CH3COO-)>c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com