
| A. | SO4-和NO3-可能来自同一工厂 | B. | Cl-和NO3-一定来自不同的工厂 | ||
| C. | Ag+和Na+可能来自同一工厂 | D. | Na+和NO3-来自同一工厂 |
分析 Ag+、Fe3+均OH-结合生成沉淀,不能共存,SO42-与Ba2+结合生成沉淀,Ag+、Cl-结合生成沉淀,不能共存,结合各含4种离子来解答.
解答 解:Ag+、Fe3+均OH-结合生成沉淀,SO42-与Ba2+结合生成沉淀,Ag+、Cl-结合生成沉淀,不能共存,
则一个厂含Ba2+、Ag+、Fe3+、NO3-,
另一个厂含Na+、Cl-、SO42-、OH-,
将两厂的污水按一定的比例混合,沉淀后污水便变成无色澄清的溶液而排放,污染程度会大大降低,
显然只有B合理,
故选B.
点评 本题考查常见离子的检验,为高频考点,把握离子之间的反应、离子共存为解答关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.


科目:高中化学 来源: 题型:实验题
| t/s | 0 | 500 | 1000 |
| c(N2O5/mol/L) | 5.00 | 3.50 | 2.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂是人体不可缺少的营养物质 | |
| B. | 油脂的水解产物是氨基酸 | |
| C. | 油脂主要在小肠中被消化吸收 | |
| D. | 脂肪中多不饱和酸含量越高,其营养价值也越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
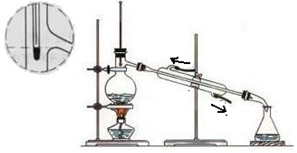
| A. | 冷凝水的进出口方向正确 | B. | 应选用20 mL的蒸馏烧瓶 | ||
| C. | 温度计液泡应插在混合液中 | D. | 锥形瓶中收集到的是甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉的作用是点燃时可以置换出氧气 | |
| B. | 在反应中NH4ClO4仅起到氧化剂作用 | |
| C. | 该反应属于分解反应,也属于氧化还原反应 | |
| D. | 上述反应瞬间能产生高温,高温是推动飞船飞行的主要因素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠可以用呼吸面具中供氧剂 | |
| B. | 氧化铝的熔点高,可用作耐火材料 | |
| C. | 铝热反应原理是炼铁最常见的反应原理 | |
| D. | 青铜是我国使用最早的合金 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com