
常温下,将pH和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,pH随溶液体积变化如图,下列有关叙述正确的是
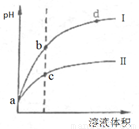
A.曲线I为醋酸稀释时pH值变化曲线
B.a点时,若都加入相同大小的锌粒,此时盐酸反应的速率大
C.a点时,若都加入足量的锌粒,最终与醋酸反应产生的氢气多
D.b点溶液中水的电离程度比c点溶液中水的电离程度小
C
【解析】
试题分析:稀释能促进弱酸电离平衡向电离方向移动,则稀释相同倍数时,盐酸pH的变化程度大于醋酸,所以图中I表示盐酸,II表示醋酸,故A错误;Zn+2H+=Zn2++H2↑,a点时盐酸和醋酸的pH相同,则c(H+)相同,因此反应速率相等,故B错误;a点时盐酸和醋酸的c(H+)相同,但前者的电离程度大于后者,则c(HCl)<c(CH3COOH),因此n(HCl)<n(CH3COOH),所以醋酸与足量锌粒反应放出的氢气多,故C正确;H2O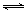 H++OH-,b点的pH大于c点的pH,则b点的c(H+)小于c点的c(H+),酸电离出的c(H+)越大,水的电离平衡越向左移动,水的电离程度越小,则b点水的电离程度大于c点,故D不正确。
H++OH-,b点的pH大于c点的pH,则b点的c(H+)小于c点的c(H+),酸电离出的c(H+)越大,水的电离平衡越向左移动,水的电离程度越小,则b点水的电离程度大于c点,故D不正确。
考点:考查强弱电解质、溶液的pH、弱酸的电离平衡、水的电离平衡、化学反应速率的大小比较等。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| H | + 4 |
| H | + 4 |
| H | + 4 |
| H | + 4 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省惠州市高三第三次调研考试理综化学试卷(解析版) 题型:选择题
常温下,将 pH和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,pH随溶液体积变化如下图,下列有关叙述正确的是
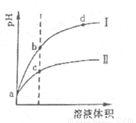
A.曲线I为醋酸稀释时pH值变化曲线
B.a点时,若都加入相同大小的锌粒,此时与盐酸反应的速率大
C.a点时,若都加入足量的锌粒,最终与醋酸反应产生的氢气多
D.b点溶液中水的电离程度比c点溶液中水的电离程度大
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
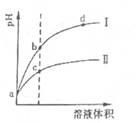
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com