
【题目】NaNO2一种食品添加剂,它致癌。酸性KMnO4溶液与NaNO2的反应方程式是MnO4-+NO2-+![]() →Mn2++NO3-+H2O。下列叙述中正确的是( )
→Mn2++NO3-+H2O。下列叙述中正确的是( )
A.该反应中NO2-被还原
B.反应过程中溶液的pH减小
C.生成1molNaNO3需消耗0.4 mol KMnO4
D.![]() 中的粒子是OH-
中的粒子是OH-
【答案】C
【解析】
该反应中Mn元素化合价由+7价变为+2价,所以MnO4-是氧化剂,NO2-应该作还原剂,亚硝酸根离子中N元素应该失电子化合价升高,酸性条件下,应该生成硝酸根离子,根据转移电子相等、原子守恒配平方程式为2MnO4-+5NO2-+6H+=2Mn2++5 NO3-+3H2O;
A.该反应中N元素化合价由+3价变为+5价,所以亚硝酸根离子失电子被氧化,故A错误;
B.根据元素守恒、电荷守恒知,□是H+,氢离子参加反应导致溶液中氢离子浓度降低,则溶液的pH增大,故B错误;
C.根据转移电子守恒得,生成1molNaNO3需消耗KMnO4的物质的量=![]() =0.4mol,故C正确;
=0.4mol,故C正确;
D.由B分析可知,□是H+,故D错误;
故答案为C。


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
【题目】在锌铜原电池池中,如图
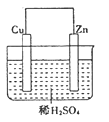
(1)锌为______极,发生的______反应,电极反应式_________________________________,观察到的现象是_______________。
(2)铜为______极,发生的______反应,电极反应式 ______________,观察到的现象是__。
(3)阳离子移向_______________极。
(4)电子从 ______________流向极到 _______________极。
(5)当电路中转移0.2mol电子,消耗硫酸的质量是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是重要的工业原料,现有![]() 、
、![]() 组成的混合物,某研究性学习小组为了探究其组成情况,取
组成的混合物,某研究性学习小组为了探究其组成情况,取![]() 该混合物加入
该混合物加入![]() 的稀硝酸中,固体物质完全反应,生成
的稀硝酸中,固体物质完全反应,生成![]() (标准状况)的
(标准状况)的![]() 。向所得溶液中加入
。向所得溶液中加入![]() 的
的![]() 溶液,恰好使溶液中的
溶液,恰好使溶液中的![]() 沉淀完全。
沉淀完全。
(1)![]() 与稀硝酸反应的化学方程式为____________。
与稀硝酸反应的化学方程式为____________。
(2)混合物中,![]() ______;
______;![]() ________。
________。
(3)![]() ______
______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:

下列说法不正确的是
A. 甲、乙、丙三种物质都含有氮元素 B. 反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C. Ⅵ的产物可在上述流程中被再次利用 D. 丁为NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 W、X、Y、Z原子序数依次增大,W与Y、X与Z位于同一主族,W与X可形成共价化合物 WX2,Y原子内层电子总数是其最外层电子数的2.5倍。下列叙述不正确的是( )
A. WX、WX2、ZX2的化学键类型完全相同
B. WZ2分子中所有原子最外层都满足8电子结构
C. 由于X的常见氢化物(H2X)分子间存在氢键,故H2X比H2Z 稳定
D. 原子半径大小顺序为X<W<Z<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且A原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满。回答下列问题:
(1)B、C中第一电离能较大的是__ (用元素符号填空),基态E原子价电子的轨道表达式______。
(2)DA2分子的VSEPR模型是_____。
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
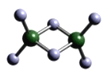
①C2Cl6属于_______晶体(填晶体类型),其中C原子的杂化轨道类型为________杂化。
②[C(OH)4]-中存在的化学键有________。
a.离子键 b.共价键 c.σ键 d.π键 e.配位键 f.氢键
(4)B、C的氟化物晶格能分别是2957 kJ/mol 、5492 kJ/mol,二者相差很大的原因________。
(5)D与E形成化合物晶体的晶胞如下图所示:
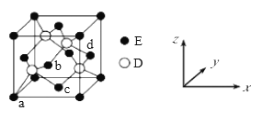
①在该晶胞中,E的配位数为_________。
②原子坐标参数可表示晶胞内部各原子的相对位置。上图晶胞中,原子的坐标参数为:a(0,0,0);b(![]() ,0,
,0,![]() );c(
);c(![]() ,
,![]() ,0)。则d原子的坐标参数为______。
,0)。则d原子的坐标参数为______。
③已知该晶胞的边长为x cm,则该晶胞的密度为ρ=_______g/cm3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A. 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B. 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C. 由氯代环己烷消去制环己烯;由丙烯加溴制![]() 二溴丙烷
二溴丙烷
D. 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞作指示剂)的滴定曲线,下列说法正确的是
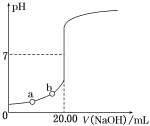
A. 水电离出的氢离子浓度:a<b
B. 盐酸的物质的量浓度为0.010 0 mol·L-1
C. 指示剂变色时,说明盐酸与NaOH恰好完全反应
D. 当滴加NaOH溶液为10.00 mL时,该混合液的pH=1+lg 3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有 X、Y、Z 三种元素,X 是有机化合物中必含的元素, Y 是地壳里含量最多的元素,Z 是质量最轻的元素。X、Y、Z 三种元素组成的有机物 M 能被酸性高锰酸钾氧化生成 N。为了测定有机物 M 的结构,做如下实验:
①将 4.6 g 有机物 M 完全燃烧,测得生成 0.2mol CO2 和 5.4 g 水;
②用质谱仪检测有机物 M,得到如图一所示的质谱图;
③用核磁共振仪处理有机物 M,得到如图二所示图谱,图中三个峰面积之比为1:2:3
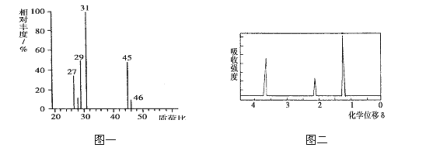
试回答下列问题:
⑴M 的结构简式是______________。
⑵N 中含有的官能团的结构简式为_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com