
【题目】下列说法不正确的是
A. 氢气的摩尔质量是2g/mol B. 摩尔是物质的量的单位
C. 1molOH—的质量是17g D. 1mol气体所占的体积约为22.4L
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列电离方程式,书写正确的是()
A. H2SO4=2H++SO42- B. NH3·H2O=NH4++OH-
C. H2CO3=H2O+CO2↑ D. H2CO3![]() 2H++CO32-
2H++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国康奈尔大学的研究人员提出的可呼吸二氧化碳电池入选美国2016年十大创新术。 电池的工作原理如图所示。下列说法不正确的是( )
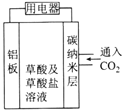
A. 该装置可将化学能转变成电能
B. 正极的电极反应式为2CO2+2e-=C2O42-
C. 利用该装置不但可减少CO2的排放,还可利用二氧化碳资源
D. 该装置中的两电极材料均被消耗,需定期补充、更换
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20 mL 0.5 mol·L-1硫酸溶液中逐滴加入烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的说法错误的是
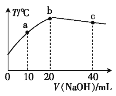
A. b点之前温度升高是因为发生了放热反应
B. bc段温度降低是因为与外界发生了热交换
C. c(NaOH)=0.5 mol·L-1
D. b点时酸碱恰好反应完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性条件下,KMnO4与H2C2O4发生氧化还原反应,用0.1 mol·L1的KMnO4与过量的H2C2O4反应,测得Mn2+的生成速率v与时间t的趋势如图,下列说法正确的是( )

A. 该反应中每生成1 mol CO2转移电子为10 mol
B. 方程式配平后,H2O的系数为6
C. 反应开始很短一段时间内v减小是因为反应物浓度减小,后来突然增大是因为生成的Mn2+对该反应有催化作用
D. t0时,Mn2+的浓度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是

A. Ka2(H2X)的数量级为10-6
B. 曲线N表示pH与 的变化关系
的变化关系
C. NaHX溶液中c(H+)>c(OH-)
D. 当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示。

(1)从反应开始到10 s,用Z表示的反应速率为______________,X的物质的量浓度减少了______________,Y的转化率为____________。
(2)该反应的化学方程式为__________________________________________________。
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是________。

A.t1时刻,减小了Z的浓度 B.t1时刻,降低了体系温度
C.t1时刻,增大了容器体积 D.t1时刻,使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的消毒剂,可用ClO2为原料制取。某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
已知:饱和NaClO2溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时 NaClO2分解成NaClO3和NaCl。Ba(ClO2)2可溶于水。
利用图所示装置进行实验。

(1)装置①的作用是___________________,装置③的作用是________________。
(2)装置②中制备ClO2的化学方程式为___________________________;装置④中反应生成NaClO2的化学方程式为_____________________。
(3)从装置④反应后的溶液中获得NaClO2晶体的操作步骤为:①减压,55 ℃蒸发结晶;②趁热过滤;③__________________;④低于60 ℃干燥,得到成品。如果撤去④中的冷水浴,可能导致产品中混有的杂质是______________。
(4)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4,操作与现象是取少量晶体溶于蒸馏水,__________________________________________________________。
(5)为了测定NaClO2粗品的纯度,取10.0 g上述初产品溶于水配成1 L溶液,取出10 mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20 mol·L-1的Na2S2O3标准液滴定,重复2次,平均消耗Na2S2O3溶液20.00 mL,计算得NaClO2粗品的纯度为_____。(提示:2Na2S2O3+I2=Na2S4O6+2NaI)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com