
【题目】元素单质及其化合物有广泛用途,请回答下列问题:
(1)第三周期元素中,钠原子核外有_______种能量不同的电子;氯原子的最外层电子排布式为______________;由这两种元素组成的化合物的电子式为__________。
(2)下列气体能用浓硫酸干燥的是________。
A.NH3 B.HI C.SO2 D.CO2
(3)请用一个实验事实说明钠与镁的金属性强弱________________________________。
(4)KClO3可用于实验室制O2,若不加催化剂,400 ℃时可分解生成两种盐,化学方程式为:KClO3 ![]() KCl+KClO4 (未配平),则氧化产物与还原产物的物质的量之比为_________。
KCl+KClO4 (未配平),则氧化产物与还原产物的物质的量之比为_________。
(5)已知:
化合物 | MgO | MgCl2 |
类型 | 离子化合物 | 离子化合物 |
熔点/℃ | 2800 | 714 |
工业上电解MgCl2制单质镁,而不电解MgO的原因是________________________________。
【答案】 4 3s23p5 ![]() CD NaOH的碱性强于氢氧化镁(或者钠与水反应更剧烈),所以钠的金属性比镁强 3:1 MgO的熔点高,熔融时耗费能源多,生产成本高
CD NaOH的碱性强于氢氧化镁(或者钠与水反应更剧烈),所以钠的金属性比镁强 3:1 MgO的熔点高,熔融时耗费能源多,生产成本高
【解析】本题分析:本题主要考查氯元素的化合物的性质。
(1)同一能级的电子能量相同,钠原子的电子占据1s、2s、2p、3s4个能级,所以其核外有4种能量不同的电子;氯原子的最外层电子排布式为3s23p5;由这两种元素组成的化合物是氯化钠,其电子式为![]() 。
。
(2)A.NH3与浓硫酸化合而不能用浓硫酸干燥;B.HI被浓硫酸氧化而不能用浓硫酸干燥;C.SO2能用浓硫酸干燥;D.CO2能用浓硫酸干燥。故选CD。
(3)NaOH的碱性强于氢氧化镁(或者钠与水反应更剧烈),所以钠的金属性比镁强。
(4) 氯元素化合价的变化为:+5→-1,+5→+7,则氧化产物与还原产物的物质的量之比为3:1。
(5)工业上电解MgCl2制单质镁,而不电解MgO的原因是MgO的熔点高,熔融时耗费能源多,生产成本高。


科目:高中化学 来源: 题型:
【题目】某硫酸厂用以下几种方法处理SO2尾气。
(1)亚硫酸钠吸收法
① Na2SO3溶液吸收SO2的离子方程式为_______________;其产物的溶液中离子浓度由大到小的排列顺序为______________。
② 常温下,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是_______
(填序号)
a.c(Na+)+c(H+)>c(SO32-)+c(HSO3-)+c(OH-)
b.c(Na+)=c(SO32-)+c(HSO3-)+C(H2SO3)
c.c(Na+)>c(SO32-)>c(OH一)>c(H+)
d.水电离出c(OH一)=1×l0-8mol/L
③25 ℃时,H2SO3![]() HSO
HSO![]() +H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=______mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=______mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中![]() 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。
(2)电化学处理法

如图所示,Pt(1)电极的反应式为_________;碱性条件下,用Pt(2)电极排出的S2O42-溶液吸收NO2,使其转化为N2,同时有SO32-生成。若阳极转移电子6mol,则理论上处理NO2气体____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是

选项 | ① | ② | ③ | 实验结论 |
A | 浓氨水 | NaOH | 酚酞试液 | 碱性:NaOH>NH3·H2O |
B | 浓硫酸 | 蔗糖 | 品红溶液 | 浓硫酸具有脱水性、氧化性 |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐反应均可生成白色沉淀 |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将224 L氯化氢气体溶于635 mL的水(密度为1.00 g/cm3)中,所得盐酸的密度为1.18 g/cm3。求:
(1)该盐酸的溶质质量分数是多少?
(2)取这种盐酸10.0 mL,稀释到1.00 L,所得的稀盐酸的物质的量浓度多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》中“黄连”条目下记载:“吐血不止,用黄连一两,捣碎,加鼓二十粒,水煎去渣,温服。”该过程中没有涉及的操作是
A. 分液 B. 加热 C. 称量 D. 过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了前20号元素中的某些元素性质的有关数据

下列有关叙述正确的是
A. 以上10种元素的原子中,失去核外第一个电子所需能量最少的是⑧
B. 由⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是PCl5和CCl4
C. 某元素R的原子半径为1.02×10-10 m,该元素在周期表中位于第三周期第ⅤA族
D. 若物质Na2R3是一种含有非极性共价键的离子化合物,则其化合物的电子式![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次递增, a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法错误的是
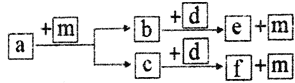
A. 简单离子半径:Z>Y
B. Z2Y2中既含有离子键又含有共价键,其中阳离子和阴离子的比值为2∶1
C. 简单气态氢化物的热稳定性:Y>X
D. 由上述4种元素组成的化合物属于离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列说法不正确的是( )
A. 硫化氢气体不能用浓硫酸干燥,是因为硫化氢有还原性
B. 医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于酸
C. 硫燃烧生成二氧化硫,是因为硫有还原性
D. 因为硫有氧化性,则硫与铁反应生成硫化铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com