
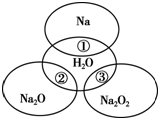
 如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、Na2O2中阴阳离子数目之比为1:1 |
| B、反应①的离子方程式为Na+2H2O═Na++2OH-+H2↑ |
| C、反应③最多能转移0.1 mol电子 |
| D、①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③ |
| 1 |
| 2 |
| 1 |
| 2 |
| 4g |
| 100g+2.2g |
| 8g |
| 100g+6.2g |
| 8g |
| 100g+6.2g |


科目:高中化学 来源: 题型:
| A、反应②在任何温度下均能自发进行 |
| B、CO(g)+2H2(g)=CH3OH(g)△H>-90.5 mol?L-1 |
| C、甲醇的标准燃烧热为△H=-764 kJ?mol-1 |
| D、若CO的标准燃烧热为△H=-282.5 kJ?mol-1,则H2标准燃烧热为△H=-286 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜.某研究性学习小组模拟工业法对铝片表面进行氧化处理.分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30min,即可得到更加致密的氧化膜.下列有关说法正确的是( )
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜.某研究性学习小组模拟工业法对铝片表面进行氧化处理.分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30min,即可得到更加致密的氧化膜.下列有关说法正确的是( )| A、电解时电子从电源负极→导线→铝极,铅极→导线→电源正级 |
| B、在电解过程中,H+向阳极移动,SO42-向阴极移动 |
| C、电解过程阳极周围溶液的pH下降 |
| D、电解的总反应为2Al+6H+═2Al3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4(HCl):AgNO3溶液、过滤 |
| B、KNO3(K2SO4):Ba(NO3)2溶液、过滤 |
| C、Cu(CuO):盐酸、过滤 |
| D、CaCO3(CaO):水、过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇.如图是实验室中模拟工业原理制取无水乙醇的装置.
工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇.如图是实验室中模拟工业原理制取无水乙醇的装置.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①>②>④>③ |
| B、①>②>③>④ |
| C、④>①>③>② |
| D、④>①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④⑥ | B、②③④⑥ |
| C、③④⑤⑥ | D、②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| MX |
| VN |
| A、以g为单位V L该气体的质量 |
| B、以g为单位1L该气体的质量 |
| C、1 L该气体中所含的分子数 |
| D、以L为单位lmol该气体的体积 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com