
| A. | 聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 | |
| B. | 高纯度的二氧化硅广泛用于制作光导纤维,遇强碱会“断路” | |
| C. | 煤经过气化和液化两种物理变化,可变为清洁能源 | |
| D. | 加热能杀死甲型H1N1流感病毒,主要是加热后使病毒中的蛋白质变性 |
分析 A.聚乙烯是无毒的高分子化合物;
B.高纯度的二氧化硅广泛用于制作光导纤维,二氧化硅能够和强碱溶液反应;
C.煤的气化和液化是化学变化;
D.加热能使蛋白质变性.
解答 解:A.聚乙烯是无毒的高分子化合物,可制作食品包装袋、食物保鲜膜,故A正确;
B.二氧化硅能够和强碱溶液反应,光导纤维遇强碱会“断路”,高纯度的二氧化硅广泛用于制作光导纤维,故B正确;
C.煤的气化是煤与水蒸汽反应H2、CO等气体的过程.煤的液化是将煤与H2在催化剂作用下转化为液体燃料或利用煤产生的H2和CO通过化学合成产生液体燃料或其他液体化工产品的过程,两种过程都生成了新物质,是化学变化,故C错误;
D.病毒的成分是蛋白质,加热能使蛋白质变性,故D正确.
故选C.
点评 本题考查聚乙烯、蛋白质的变性、煤的气化和液化、光导纤维等,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 都能使溴水和酸性高锰酸钾溶液褪色 | |
| B. | 都能发生加聚反应生成高分子化合物 | |
| C. | 都不溶于水,且密度比水小 | |
| D. | 分子中各原子都处于同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol/L的NaHCO3溶液中HCO3-和CO3 2-离子数之和为0.1NA | |
| B. | 标准状况下,22.4LC2H4与C3H6混合气体所含有分子数为NA | |
| C. | 1molNa2O2与足量的CO2反应转移的电子数为2NA | |
| D. | 18gNH4+所含的电子数11NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Cu(OH)2 | Mg(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀的pH | 4.8 | 9.3 | 2.7 | 3.8 |
| 完全沉淀的pH | 6.4 | 10.8 | 3.7 | 4.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 测定次数 | 盐酸的体积/mL | KOH溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 这类电池的正极反应与金属的吸氧腐蚀正极反应相似 | |
| B. | 每转移1mol电子则这种电池产生电能为0.5度电 | |
| C. | 电池的负极反应为:CH4+10OH-═CO32-+7H2O+8e- | |
| D. | 当消耗0.4mol燃料时,电池中的各种离子的浓度关系为:C(K+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.4g乙烯与丙烯的混合气体含有NA个碳原子 | |
| B. | 精炼铜,若阳极失去2NA个电子,则阴极增重64g | |
| C. | 在1L 0.1mol/L的Na2CO3溶液中,阴离子总数小于0.1NA | |
| D. | 将1L 2mol/L的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
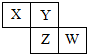
| A. | W的原子序数不可能是X的原子序数的3倍 | |
| B. | Z元素可能是金属元素 | |
| C. | W的气态氢化物的稳定性一定比Y的强 | |
| D. | 四种元素的原子有可能均能与氢原子形成18电子分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com