
������( Be)���仯����������ƵĻ�ѧ���ʡ���֪��BeCl2 +Na2BeO2 +2H2O=2NaCl+2Be��OH)2������ȫ���У��������ƶ���ȷ����
A��Be(OH)2�����������ᣬ��������NaOH��Һ
B��BeCI2ˮ��Һ�ĵ�����ǿ����BeCl2�����ӻ�����
C��Na2BeO2��Һ��pH>7���������ɲ����պ�õ��IJ�����ΪBeO
D��BeCl2��Һ��pH>7���������ɲ����պ�õ��IJ����������BeCl2

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ���˴�һ�и���7��������ѧ�Ծ��������棩 ���ͣ�ѡ����
ˮ�ȷ��Ʊ�Fe3O4�������ķ�ӦΪ3Fe2����2S2O32-��O2��xOH��===Fe3O4��S4O62--��2H2O������˵���д������(����)��
A��ÿ����1 mol Fe3O4����Ӧת�Ƶĵ�������Ϊ4mol
B��Fe2����S2O32-���ǻ�ԭ��
C��1 mol Fe2��������ʱ����Fe2����ԭ��O2�����ʵ���Ϊmol
D��x��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ����7�����ڽ��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ȤС�������ͼװ�ý�������������Ƶķ�Ӧ���Ƚ���Ԥ�ȣ��������ڳ�С��ʱ�����𣬲�ͨ��������������Ӧ�����������д������(����)

A������������ȼ�ղ�����ɫ�Ļ���
B����Ӧ�����Ĵ����������Ȼ��ƹ���
C������ٵ����������չ���������ֹ������Ⱦ
D������ڱ���ɫ��֤�������ѱ���Һ��ȫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��ɳ�и�����ѧ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Ԫ��X��Y��Z��W��ԭ�����������������Ƿֱ�λ�ڲ�ͬ�����壬X ���������������۴�����Ϊ0��YΪ����Ԫ�أ�Y��Z����������֮����W��������������ȣ�X��W����������֮�͵���10������˵����ȷ����
A. ԭ�Ӱ뾶��С˳��r(W)>r(Z)>r(Y)>r(X)
B. �е㣺XW2>Y2W
C. ����������Ӧ��ˮ��������ԣ�X<Z
D. ���⻯������ȶ��ԣ�Z>W
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017����Ϻ������и���ʵ������ڵ�һ���¿����ۻ�ѧ�������棩 ���ͣ�ʵ����
����������18�֣���������Ϊ��ɫ���壬��Ϊһ�ֻ���ԭ�ϣ��ɹ㷺����Ϳ�ϡ��մɡ���������ȵ���ɫ���Լ����͵�ز��ϡ��й���ϵ��������ϳɲ����������������£�
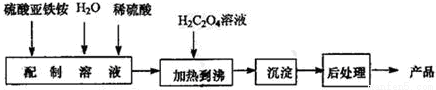
��1������(NH4)2Fe(SO4)2 6H2O��Һʱ�����������ϡ���ᣬĿ����_____________��
6H2O��Һʱ�����������ϡ���ᣬĿ����_____________��
��2���õ��IJ���������������ϴ�ӣ������Ƿ�ϴ�Ӹɾ��ķ�����_____________��
��3�����ƵõIJ�Ʒ(FeC2O4��2H2O)����������н��м��ȷֽ⣬�������ͼ(TG%��ʾ������������ռԭ��Ʒ�������İٷ���)��
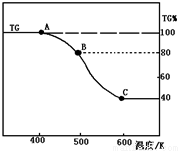
����A-B������Ӧ�Ļ�ѧ����ʽΪ_____________��
����֪B��C�������е����ʵ�����������̬���������ɣ�д��B��C�Ļ�ѧ����ʽ_____________��
��4��ij����������Ʒ�к�����������李�Ϊ�˲ⶨ������Ʒ�в�����ĺ�����ijͬѧ�������·���ʵ�飺
��ȷ����m g��Ʒ����������2mol/L�����в���100mL����ƿ���ݡ�
��ȡ������Һ20mL����c mol/L������ر���Һ�ζ�����Һ��Ϊ����ɫ�����ĸ��������Һ�����ΪV1 mL��
����������Һ�м�������Zn�ۣ�ʹ��Һ�е�Fe3+ǡ��ȫ����ԭΪFe2+�����ˡ�
����ϴ��ʣ���п�ۺ���ƿ��ϴ��Һ������Һ��
������c mol/L KMnO4��Һ�ζ�����Һ����Һ���ֵ���ɫ������KMnO4��Һ�����V2 mL��
�ش��������⣺
����֪������(H2C2O4)�����Ը��������Һ��Ӧ�������������ݲ�������ɫ��ʧ��д���÷�Ӧ�����ӷ���ʽ��_____________��
����ʡ�Բ��������ⶨ�IJ�������Ӻ��� (�ƫ����ƫС�����䡱)��
��m g��Ʒ�в�������ӵ����ʵ���Ϊ_____________(��c��V1��V2��ʽ�ӱ�ʾ�����ػ���)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�����и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ������
�⻯��ͭ��Cu2I2����һ�ֲ�����ˮҲ��������İ�ɫ���壬��;�ܹ㷺�����������գ�
��1���⻯����Һ�еμ���������ͭ��Һ�����ܵõ��⻯��ͭ��д���÷�Ӧ�Ļ�ѧ����ʽ ��
��2����������Ӧ����Һ�м�����ۣ���Һ�������ٵμ���������Һ����ɫ����ȥ��д��KI��Cu2I2��H2SO3�Ļ�ԭ����ǿ������˳���� ��
��3���⻯��ͭ�����ڼ������еĹ��������䷴ӦΪ��2Cu2I2+Hg�TCu2HgI4��õ��죩+2Cu������Cu2HgI4��CuԪ���� �ۣ�����1molCu2I2���뷴Ӧʱ��ת�Ƶ��� mol��
��4��Ϊ��ȥϡ����������CuCl2���ʣ�������Һ�м��������M�Լ�����й��˲�������ͨ��������Cl2�����N�������Լ�M�Ͳ���N�������ȷ���� ��ѡ���ţ�
ѡ�� | �Լ�M | ����N |
a | �⻯����Һ | ���� |
b | �������Һ | ��ȡ��Һ |
c | ���� | ���� |
d | ��������Һ | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�����и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���ֶ���������Ԫ��A��B��C��D��E��ԭ���������ε�����A2������ɫȼ�ϣ�C�������ﳣ���ڲ�����������DԪ��ԭ�ӵĺ˵������ͬ������һ����Ԫ�ص�2����B��CΪͬ����Ԫ�أ�B��Dԭ������������֮�͵���E�������������� ������������������˵������ȷ���ǣ� ��
A. ����Ԫ����BԪ�صĽ�������ǿ
B. Ԫ��D��E�ֱ���Ԫ��A�γɻ�������ȶ��ԣ�A2D��AE
C. Ԫ��C��D��E������������Ӧˮ��������Եݼ�
D. Ԫ��B��D��E�ļ����Ӱ뾶��СΪ��B��D��E
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ӱ������и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
(10��)KNO3����Ҫ�Ļ�����Ʒ��������һ���ѻ��ר����KNO3�Ʊ���������Ҫ���裺
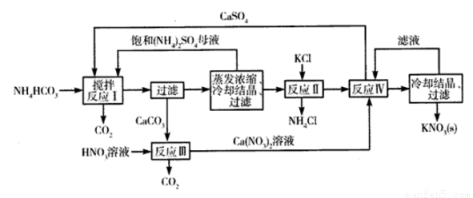
��1����ӦI�У�CaSO4��NH4HCO3�����ʵ���֮��Ϊ1��2���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2����Ӧ�����ڸ�̬�����ȵ������½��У����ȵ�Ŀ���� �� �ӷ�Ӧ�����û�����з����CaSO4�ķ����dz��ȹ��ˣ����ȹ��˵�Ŀ���� ��
��3�����鷴Ӧ������K2SO4���Ƿ����KCl�ķ����ǣ�ȡ����K2SO4��Ʒ�ܽ���ˮ�� ��
��4�����������У���ѭ�����õ����ʳ�(NH4)2SO4�⣬���� �� (�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017����ϳ�ɳһ�и߶��ϵ�һ���¿�����ѧ���ԣ���ѧ���������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A�����������Һ��ͨ������Ķ�����̼ Ca2++2ClO��+H2O+CO2�TCaCO3��+2HClO
B������������Һ�м������������Һ Fe2++2H2O2+4H+�TFe3++4H2O
C���ð�ˮ���������������� OH��+SO2�THSO3��
D����������Һ���������ˮ 3NH3•H2O+Fe3+�TFe��OH��3��+3 NH4+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com