
已知Zn(OH)2的溶度积常数为1.2×10-17,则Zn(OH)2在水中物质的量浓度为( )
A.1.4×10-6 mol·L-1 B.2.3×10-6 mol·L-1
C.1.4×10-9 mol·L-1 D.2.3×10-9 mol·L-1
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案科目:高中化学 来源:2014-2015学年河南省高三12月月考化学试卷(解析版) 题型:选择题
下列有关化学用语正确的是
①乙烯的最简式C2H4 ②乙醇的结构简式C2H6O
③四氯化碳的电子式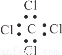 ④乙炔的结构简式CHCH
④乙炔的结构简式CHCH
⑤乙烷的结构式CH3CH3 ⑥乙醛的结构简式CH3COH
A.全对 B.全错 C.③④⑤ D.③④⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三第五次调研考试化学试卷(解析版) 题型:简答题
(14分)甲醇是一种重要的化工原料,在生产中有着重要的应用。工业上用甲烷氧化法合成甲醇的反应有:
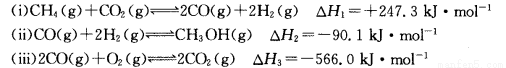
(1)用CH4和02直接制备甲醇蒸气的热化学方程式为 。
(2)某温度下,向4 L恒容密闭容器中通人6 mol C02和6mol CH4,发生反应(i),平衡体系中各组分的体积分数均为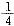 ,则此温度下该反应的平衡常数K= ,CH4的转化率为 。
,则此温度下该反应的平衡常数K= ,CH4的转化率为 。
(3)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为:
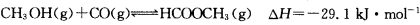 ,科研人员对该反应进行了研究,部分研究结果如下:
,科研人员对该反应进行了研究,部分研究结果如下:


①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是 (填“3.5× 106 Pa” “4.O×106 Pa”或“5.0× 106 Pa”)。
②实际工业生产中采用的温度是80℃,其理由是 。
(4)直接甲醇燃料电池(简称DMFC)由于其结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:

①通入a气体的电极是电池的 (填“正”或“负”)极,其电极反应式为 .
②常温下,用此电池以惰性电极电解O.5 L饱和食盐水(足量),若两极共生成气体1.12 L(已折算为标准状况下的体积),则电解后溶液的pH为 (忽略溶液的体积变化)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三第三次调研考试化学试卷(解析版) 题型:选择题
用NA表示阿伏伽德罗常数的值。下列叙述正确的是:
A.常温常压下,22.4L CH4中含有4NA个C-H键
B.48g O3气体含有3NA个氧原子
C.在1L0 .5mol·L-lFeCl3溶液中含有0.5NA个Fe3+
D.标准状况下,2.24LCCl4含有的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是
A.乙醇在电池的负极上参加反应
B.1mol CH3CH2OH被氧化转移6mol e-
C.随着反应的进行,正极附近的酸性减弱。
D.电池正极的正极反应为4H++O2+4e-=2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若A、B相连A为负极;C、D相连D上有气泡逸出;A、C相连A 被腐蚀;B、D相连,B被保护。则四种金属的活泼性顺序由大到小排列为
A.A>B>C>D B.A>C>B>D
C.A>C>D>B D.B>D>C>A
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列常见金属的冶炼原理中不合理的是
金属 | 冶炼原理 | |
A | Fe | Fe2O3+3CO= |
B | Hg | 2HgO |
C | Mg | 2MgO(熔融)= |
D | Na | 2NaCl(熔融)= |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省濉溪县高三第二次月考化学试卷(解析版) 题型:选择题
向四支盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如下图所示:

则下列分析都正确的组合是
选项 | 溶质的成分 | 对应图象 | 溶液中离子浓度关系 |
A | NaHCO3 | I | c(Na+) = c(HCO3-) |
B | NaOH、Na2CO3 | Ⅳ | c(OH-)>c(CO32-) |
C | Na2CO3 | Ⅲ | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
D | NaHCO3、Na2CO3 | Ⅱ | c(CO32-)>c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期中化学试卷(解析版) 题型:选择题
化学方程式可简明地体现元素及其化合物的性质。
已知:

下列说法不正确是:
A.酸性(水溶液):HSCN〉H2CO3〉HCN
B.还原性(碱性溶液):Fe(OH)2〉I—〉KIO3
C.热稳定性:NaCl〉NaClO4〉NaClO
D.氧化性(酸性溶液):I2〉FeCl3〉Co(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com