
(14��)�״���һ����Ҫ�Ļ���ԭ�ϣ���������������Ҫ��Ӧ�á���ҵ���ü����������ϳɼ״��ķ�Ӧ�У�
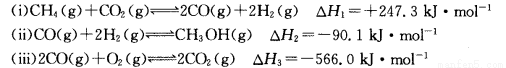
(1)��CH4��02ֱ���Ʊ��״��������Ȼ�ѧ����ʽΪ ��
(2)ij�¶��£���4 L�����ܱ�������ͨ��6 mol C02��6mol CH4��������Ӧ(i)��ƽ����ϵ�и���ֵ����������Ϊ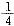 ������¶��¸÷�Ӧ��ƽ�ⳣ��K= ��CH4��ת����Ϊ ��
������¶��¸÷�Ӧ��ƽ�ⳣ��K= ��CH4��ת����Ϊ ��
(3)��ҵ�Ͽ�ͨ���״��ʻ�������ȡ����������䷴Ӧ���Ȼ�ѧ����ʽΪ��
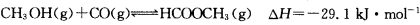 ��������Ա�Ը÷�Ӧ�������о��������о�������£�
��������Ա�Ը÷�Ӧ�������о��������о�������£�


�ٴӷ�Ӧѹǿ�Լ״�ת���ʵ�Ӱ�조Ч�ʡ�������ҵ��ȡ�������Ӧѡ���ѹǿ�� (�3��5�� 106 Pa�� ��4��O��106 Pa����5.0�� 106 Pa��)��
��ʵ�ʹ�ҵ�����в��õ��¶���80�棬�������� ��
(4)ֱ�Ӽ״�ȼ�ϵ��(���DMFC)������ṹ������ת���ʸߡ��Ի�������Ⱦ������Ϊ������Դ�����Ʒ��Խ��Խ�ܵ���ע��DMFC�Ĺ���ԭ����ͼ��ʾ��

��ͨ��a����ĵ缫�ǵ�ص� (���������)������缫��ӦʽΪ .
�ڳ����£��ô˵���Զ��Ե缫���O��5 L����ʳ��ˮ(����)������������������1��12 L(������Ϊ��״���µ����)���������Һ��pHΪ (������Һ������仯)��
��1��2CH4��g��+02(g)2CH3OH(g) ��H��-251.6 kJ/mol
��2��1 33.3%
��3����4.0��106Pa��
��80��ʱ���ʴ��Ҹ���80��ʱ���ʱ仯�����ԣ�����Ϊ���»�ѧƽ�������ƶ���ת���ʽ��͡�
��4���ټ״���CH3OH-6e-+H2O=CO2+6H+
��13
��������
�����������1���ɸ�˹����֪(i)��2+(ii)��2+(iii)��2CH4��g��+02(g)2CH3OH(g) ���H����+247.3kJ/mol����2+��-90.1 kJ/mol����2+��-566.0 kJ/mol��=-251.6 kJ/mol��2����������ʽ���跴Ӧ����CH4���ʵ���Ϊn
CH4��g��+C02(g)2CO(g)+2H2(g)
��ʼn/mol 6 6 0 0
�仯n/mol n n 2n 2n
ƽ��n/mol 6-n 6-n 2n 2n
������ã�2n/(12+2n)=1/4 ���n=2mol
K=(12��12)/(1��1)=1
COת����Ϊ(2/6)��100%=33.3%��3������ͼ��֪�� 3��5�� 106 Pa ��4��O��106 Pa ֮��״�ת������������ԣ���4.0��106Paʱ�״�ת�����Ѿ��ϸߣ��ʹ�ҵ��ȡ�������ѡ���ѹǿΪ4.0��106Pa����ͼ����80��ʱ���ʴ��Ҹ���80��ʱ���ʱ仯�����ԣ�����Ϊ�÷�ӦΪ���ȷ�Ӧ���²�����Ӧ������У�����ʵ�ʲ��õ��¶���80�档��4������DMFC�Ĺ���ԭ��ͼʾ�����ݵ������������ж�aΪ����ͨ���Ϊ�״����缫��Ӧ����ʽΪ��CH3OH-6e-+2H2O=CO2+6H+�ڶ��Ե缫���O��5 L����ʳ��ˮ����������������0.05mol��������������0.025mol�ɷ�Ӧ2Cl-+2H2O=Cl2��+H2��+2OH-�ɵ�C��OH-��=0.05mol/0.5L=0.1mol/L����PH��13
���㣺�����˹���ɣ��������ø�˹���ɽ����йط�Ӧ�ʱ�ļ��㡣�˽⻯ѧƽ�ⳣ���ĺ��壬�����û�ѧƽ�ⳣ��������ؼ��㡣�������������Ũ�ȡ��¶ȡ�ѹǿ�������ȣ��Է�Ӧ���ʺͻ�ѧƽ���Ӱ�죬��ʶ������������۽�����һ����ɡ� �˽�ԭ��غ͵��صĹ���ԭ������д���缫��Ӧ�͵�ط�Ӧ����ʽ��


 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
1.52 gͭþ�Ͻ���ȫ�ܽ���50 mL�ܶ�Ϊ1.40 g/mL����������Ϊ63%��Ũ�����У��õ�NO2��N2O4 �Ļ������1120 mL (��״��)����Ӧ�����Һ�м���1.0 mol/L NaOH��Һ������������ȫ������ʱ���õ�2.54 g����������˵������ȷ����
A���úϽ���ͭ��þ�����ʵ���֮����2��1
B����Ũ������HNO3�����ʵ���Ũ����14.0 mol/L
C��NO2��N2O4 �Ļ�������У�NO2 �����������80%
D���õ�2.54 g����ʱ������NaOH��Һ�������600 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ����1����ϰ���ۻ�ѧ�Ծ��������棩 ���ͣ������
[��ѧ����ѡ��2����ѧ�뼼��]��15�֣���ʯ��Ҫ�������[Ca3(PO4)2 H2O]����ʯ[Ca5F(PO4)3��Ca5(OH)(PO4)3]����ʽ���ڡ�ͼ��a��ΪĿǰ��������ʯ���õĴ������������ʪ��������ָ��ʯ�ù�������ֽ��Ʊ����ᡣͼ��b�����ȷ��������ɹ���������ʯ�Ƶ��������̡�
H2O]����ʯ[Ca5F(PO4)3��Ca5(OH)(PO4)3]����ʽ���ڡ�ͼ��a��ΪĿǰ��������ʯ���õĴ������������ʪ��������ָ��ʯ�ù�������ֽ��Ʊ����ᡣͼ��b�����ȷ��������ɹ���������ʯ�Ƶ��������̡�
ͼ��a��
ͼ��b��
�������ʵ�����������£�
�۵�/�� | �е�/�� | ��ע | |
���� | 44 | 280.5 | |
PH3 | -133.8 | -87.8 | ������ˮ�����л�ԭ�� |
SiF4 | -90 | -86 | ��ˮ�� |
�ش��������⣺
��1����������ʯ����Ҫ����;�����������ϣ�Լռ��ʯʹ������ �G��
��2������ʯΪԭ�ϣ�ʪ�����������Ca3F(PO4)3��Ӧ�Ļ�ѧ����ʽΪ�� ������1���ۺϺ�������������Լ30%����ʯ�������Ƶ�85�G����Ʒ���� �֡�
��3����ͼ(b)��ʾ���ȷ���������ĵ�һ���ǽ��������衢������̿����ʯ��ϣ����·�Ӧ���ɰ��ס�¯������Ҫ�ɷ��ǣ� (�ѧʽ)������1����Ҫ�������ǣ� ������2����Ҫ�������ǣ�
��4��β������Ҫ���� ������������PH3��H2S��HF�ȣ���β����ͨ�봿����Һ���ɳ�ȥ ����ͨ�����������Һ���ɳ�ȥ (���ѧʽ)
��5�������ʪ�����ᣬ�ȷ����Ṥ�ո��ӣ��ܺĸߣ����ŵ��ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ����У������ѧ�ڵڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�������Ԥ��ʵ��Ŀ�Ļ�����ʵ�����һ�µ���
ѡ�� | ʵ����� | ʵ��Ŀ�Ļ���� |
A | ���е�������Ũ��ˮ�������� | ��Һ�ֲ㣬�ϲ�ʳȺ�ɫ���²㼸����ɫ��������ˮ����ȡ����Ӧ��ʹ��ˮ��ɫ |
B | ��������FeCl3��MgCl2��Һ�м�������Mg(OH)2��ĩ������һ��ʱ������ | ��ȥMgCl2��Һ������FeCl3 |
C | ������Һ�м��뱥��(NH4)2SO4��Һ | �а�ɫ���������������ʷ����˱��� |
D | C2H5OH��Ũ����170 �湲�ȣ��Ƶõ�����ͨ������KMnO4��Һ | �����Ƶ������Ƿ�Ϊ��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ��������ε��п��Ի�ѧ�Ծ��������棩 ���ͣ������
[��ѧ�����л���ѧ����](15��)����̪(J)�������ᡢ�жȼ�����ȱѪ��ҩ��ϳ�J��һ��·������

��E�ĺ˴Ź�������ֻ��һ��壻
��C�ܷ���������Ӧ��
��J��һ�����������г����������һ����Ԫ����
�ش��������⣺
��1����A����B�Ļ�ѧ����ʽΪ ���䷴Ӧ����Ϊ
��2��D�Ļ�ѧ������
��3��J�Ľṹ��ʽΪ ����D����E�Ļ�ѧ����ʽΪ
��4��G��ͬ���칹���к˴Ź���������4��������� ��Һ������ɫ��Ӧ�Ľṹ��ʽΪ (д��һ�ּ���)
��Һ������ɫ��Ӧ�Ľṹ��ʽΪ (д��һ�ּ���)
��5���ɼ�ȩ�ͻ�����A�����в���ɵõ�2һ�����Ҵ���

��Ӧ����1Ϊ ����Ӧ����2��ѡ����Լ�Ϊ ��L�Ľṹ��ʽΪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ��������ε��п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
W��X��Y��Z���Ƕ�����Ԫ�أ�X��Y��Z����ͬһ���ڣ�w��X��Z�ļ����Ӿ�����ͬ�ĵ��Ӳ�ṹ��W�ĵ����ǿ����к����������壬X��������������ԣ�Y���������������۵Ĵ�����ΪO������˵����ȷ����
A�������۵㣺w>Z B�����Ӱ뾶��w>x>Z
C��������ۣ�w>X>Z D��ԭ��������Z>w>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ�����и��������ε��п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ�У��������ʵ���Ũ�ȹ�ϵ��ȷ����
A��ijNa2CO3��Һ�У�c(OH��)��2c(CO32��)+c(HCO3��)��c(H��)��c(Na+)
B������ʱ����PH=1�Ĵ����PH=13��NaOH��Һ�������Ϻ����Һc(CH3COO��)��c(Na+)��c(H��) ��c(OH��)
C��NaHCO3��Һ�У�c(Na+)��2c(CO32-)��c(HCO3-)+c(H2CO3)
D��0.1 mol��L��1(NH4)2Fe(SO4)2��Һ�У�c(NH4+)��c(NH3��H2O)��0.2 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪Zn(OH)2���ܶȻ�����Ϊ1.2��10��17����Zn(OH)2��ˮ�����ʵ���Ũ��Ϊ( )
A��1.4��10��6 mol��L��1 B��2.3��10��6 mol��L��1
C��1.4��10��9 mol��L��1 D��2.3��10��9 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�갲��ʡ������У���˸�����ѧ��3���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�������Һ��pH���������ʵ���Ũ�ȹ�ϵ��ȷ����
A��0.1mol��L��1NaHCO3��Һ�е�����Ũ�ȣ�c(Na+)>c(HCO3��)>c(CO32��)>c(H2CO3)>c(OH��)>c(H��)
B���������2.24L��CO2ͨ��150mL 1mol��L-1NaOH��Һ�г�ַ�Ӧ�����Һ��2c(Na��)��3c(CO32��)��3c(HCO3��)��3c(H2CO3)
C��pH��3�Ķ�Ԫ����H2R��Һ��pH��11��NaOH��Һ��Ϻ����Һ��pH����7����Ӧ��Ļ��Һ��2c(R2��)��c(HR��)��c(Na��)
D��0.2 mol��L-1��ijһԪ��HA��Һ��0.1 mol��L-1NaOH��Һ�������Ϻ���ҺpH����7����Ӧ��Ļ��Һ��c(OH��)��2c(A��)��c(H��)��2c(HA)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com