
【题目】氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。可利用太阳能光伏电池电解水制高纯氨,工作示意图如图所示。通过控制开关连接K1和K2,可交替得到H2和O2,下列有关说法错误的是( )

A.制H2时,开关应连接K1,产生H2的电极反应式是2H2O+2e-=H2↑+2OH-
B.当开关连接K2时,电极3的反应式为Ni(OH)2-e-+OH-=NiOOH+H2O
C.当开关连接K2时,电极2作阳极,得到O2
D.电极3的作用是分别作阳极材料和阴极材料,利用NiOOH和Ni(OH)2的相互转化提供电子转移
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的原子结构示意图为_________;
(2)②的气态氢化物分子的结构式为___________,②和⑦的气态氢化物的稳定性相比,其中较弱的是____ (用该氢化物的化学式表示);
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是____(填化学式);
(4)⑤、⑥元素的金属性强弱依次为___________(填“增大”、“减小”或“不变”);
(5)④、⑤、⑥的形成的简单离子半径依次_________(填“增大”、“减小”或“不变”);
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研究发现:硫化态的钴、钼、硫相互作用相(所谓“CoMoS”相)和噻吩(分子式为C4H4S)的加氢脱硫反应(C4H4S+4H2→C4H10+H2S)活性有线性关系。请回答下列有关问题:
(1)基态钴原子的外围电子排布图(轨道表示式)为___________。
(2)常温下,噻吩是一种无色、有恶臭、能催泪的液体,天然存在于石油中。
①1mol噻吩(![]() )中含有的
)中含有的![]() 键数目为___。
键数目为___。
②在组成噻吩的三种元素中,电负性最小的是__(填元素符号,下同);与S元素位于同一周期的非金属元素第一电离能由大到小的顺序为_______________。
(3)已知沸点:H2O>H2Se>H2S,其原因 __________。
(4)H2S在空气中燃烧可生成SO2,SO2催化氧化后得到SO3。
①写出与SO2互为等电子体的分子和离子:___、___(各一种)。
②气态SO3以单分子形式存在,其分子的立体构型为_____;固态SO3形成三聚体环状结(如图1所示),该分子中S原子的杂化轨道类型为______。

(5)Na2S的晶胞结构如图2所示,则黑球代表的离子是___。已知Na![]() 的半径为0.102nm,S2-的半径为0.184nm,根据硬球接触模型,则Na2S的晶胞参数a=__nm(列出计算式即可)。
的半径为0.102nm,S2-的半径为0.184nm,根据硬球接触模型,则Na2S的晶胞参数a=__nm(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠、铝是两种重要的金属,其单质及化合物在人们的日常生活、生产及科学研究中具有广泛的用途。回答下列问题:
(1)基态铝原子的电子排布图是____________________。
(2)与Al3+具有相同的电子层结构的简单阴离子有__________(填离子符号),其中形成这些阴离子的元素中,电负性最强的是__________(填元素符号,下同),第一电离能最小的是__________。
(3)Al、Cl的电负性如下表:
元素 | Al | Cl |
电负性 | 1.5 | 3.0 |
则AlCl3为________晶体(填晶体类型);AlCl3升华后蒸气的相对分子质量约为267,则该蒸气分子的结构式是____________(标明配位键)。
(4)氢化铝钠(NaAlH4)是重要的有机合成中还原剂。
①![]() 的空间构型为____________。
的空间构型为____________。
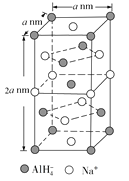
②NaAlH4的晶胞如下图所示,与Na+紧邻且等距的![]() 有________个;NaAlH4晶体的密度为________g/cm3(用含a 的代数式表示,NA代表阿伏加德罗常数)。
有________个;NaAlH4晶体的密度为________g/cm3(用含a 的代数式表示,NA代表阿伏加德罗常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列数据:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 |
乙醇 | -144 | 78.0 | 0.789 |
乙酸 | 16.6 | 118 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.900 |
浓硫酸(98%) | - | 338 | 1.84 |
下图为实验室制取乙酸乙酯的装置图。
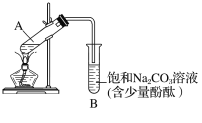
(1)当饱和碳酸钠溶液上方收集到较多液体时,停止加热,取下小试管B,充分振荡,静置。振荡前后的实验现象为________(填字母)。
A.上层液体变薄
B.下层液体红色变浅或变为无色
C.有气体产生
D.有果香味
(2)为分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行分离:

①试剂1最好选用_________________________________________________;
②操作1是________,所用的主要仪器名称是__________________________;
③试剂2最好选用_____________________________________;
④操作2是_______________________________________;
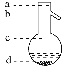
⑤操作3中温度计水银球的位置应为下图中________(填“a”“b”“c”或“d”)所示,在该操作中,除蒸馏烧瓶、温度计外,还需要的玻璃仪器有__________、________、________、________,收集乙酸的适宜温度是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种重要的有机物,可通过以下方法合成:

(1)B中含有的官能团名称为_________________。
(2)A→B的化学方程式为_________________。
(3)B→C的反应类型为_________________。
(4)E的分子式为C10H10O4N2,写出E的结构简式:______________________。
(5)写出同时满足下列条件的C的一种同分异构体的结构简式:_______________________。
①能发生银镜反应;②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;
③分子中只有4种不同化学环境的氢。
(6)已知:CH3CHO+CH3CHO![]() CH3CH=CHCHO。请结合题给信息,以苯和
CH3CH=CHCHO。请结合题给信息,以苯和![]() 为原料制备
为原料制备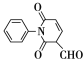 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)__________________。
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1273K、100.0kPa条件下,乙烷生成乙烯的反应C2 H6(g)![]() C2 H4(g)+H2(g)达到平衡后
C2 H4(g)+H2(g)达到平衡后
A. C2 H6的浓度保持不变
B. C2 H6仍在不断分解,其浓度不断减小
C. C2 H6的分解速率大于生成速率
D. C2 H4仍在不断生成,其浓度不断增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应方程式书写错误的是( )
A.![]() +HO-NO2(浓)
+HO-NO2(浓)![]()
![]() +H2O
+H2O
B.CH2=CH2+H2O![]() CH3CH2OH
CH3CH2OH
C.2CH3CH2OH+O2![]() 2CH3CHO
2CH3CHO
D.CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氢气是一种未来十分理想的能源。
镧镍合金是一种良好的储氢材料,在一定条件下通过如下反应实现储氢:
LaNi3(s)+3H2(g) ![]() LaNi3H6(s) H<0。 某实验室模拟该过程,向体积一定的密闭容器中充入反应物发生反应。H2的平衡转化率与其初始加入量(n)、反应温度(T)的关系如下左图所示;一定温度(T)下,将a mol的氢气充入体积是1 L的容器内,气体的压强(P)随时间(t)的变化关系如下右图所示:
LaNi3H6(s) H<0。 某实验室模拟该过程,向体积一定的密闭容器中充入反应物发生反应。H2的平衡转化率与其初始加入量(n)、反应温度(T)的关系如下左图所示;一定温度(T)下,将a mol的氢气充入体积是1 L的容器内,气体的压强(P)随时间(t)的变化关系如下右图所示:

①n1、n2、n3的大小关系是_______。
②温度T1下反应的平衡常数是__________(用含a的代数式表示)。
③保持温度不变,在t6时刻将容积压缩至原容积的一半,容器内的压强_________6kPa(填写“大于”或“小于”)。
(2)贮氢合金ThNi5可催化由CO、H2合成CH4等有机化工产品的反应。温度为TK时发生以下反应①![]()
②![]()
③![]()
![]() _______。
_______。
(3)TK时,向一恒压密闭容器中充入等物质的量的CO(g)和H2O(g)发生上述反应②(已排除其他反应干扰),测得CO(g)物质的量分数随时间变化如下表所示:

若初始投入CO为2 mol,恒压容器容积10 L,用H2O(g)表示该反应0-5分钟内的速率v[H2O(g)]=______。6分钟时,仅改变一种条件破坏了平衡,且第9min达到平衡时,CO的物质的量是0.2mol,则改变的外界条件为_________。
(4)温度、压强对反应CO(g)十2H2(g)=CH3OH(g) H=-90. 1 kJ·mol-1中CO转化率的影响如图所示:

①温度在较低范围内,对CO转化率影响的主要因素是____________ (填“温度”或“压强”)。
②由图像可知,温度越低,压强越大,CO转化率越高。但实际生产往往采用300~400 °C和10 MPa的条件,其原因是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com