
【题目】已知下列数据:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 |
乙醇 | -144 | 78.0 | 0.789 |
乙酸 | 16.6 | 118 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.900 |
浓硫酸(98%) | - | 338 | 1.84 |
下图为实验室制取乙酸乙酯的装置图。
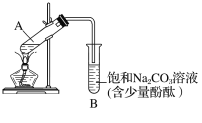
(1)当饱和碳酸钠溶液上方收集到较多液体时,停止加热,取下小试管B,充分振荡,静置。振荡前后的实验现象为________(填字母)。
A.上层液体变薄
B.下层液体红色变浅或变为无色
C.有气体产生
D.有果香味
(2)为分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行分离:

①试剂1最好选用_________________________________________________;
②操作1是________,所用的主要仪器名称是__________________________;
③试剂2最好选用_____________________________________;
④操作2是_______________________________________;
⑤操作3中温度计水银球的位置应为下图中________(填“a”“b”“c”或“d”)所示,在该操作中,除蒸馏烧瓶、温度计外,还需要的玻璃仪器有__________、________、________、________,收集乙酸的适宜温度是_______________________________________。
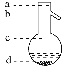
【答案】ABCD 饱和碳酸钠溶液 分液 分液漏斗 稀硫酸 蒸馏 b 酒精灯 冷凝管 牛角管 锥形瓶 略高于 118 ℃
【解析】
乙醇、乙酸的沸点较低,易挥发;根据乙酸的酸性和乙酸乙酯难溶于饱和碳酸钠分析;
(1)饱和碳酸钠溶液上方收集到较多液体包括乙酸乙酯、乙酸、乙醇。乙酸乙酯有果香味,不溶解且密度比水小,乙酸和能碳酸钠反应放出CO2气体,乙醇可以和饱和碳酸钠溶液互溶,取下小试管B,充分振荡,静置。可以产生的现象为:有果香味;上层液体变薄;下层液体红色变浅或变为无色;同时有气体产生。所以A B C D均符合题意;答案:A B C D。
(2)①制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,所以试剂1最好选用饱和碳酸钠溶液,因此,本题正确答案是:饱和碳酸钠溶液;
②乙酸乙酯不溶于碳酸钠溶液,所以混合液会分层,可以通过分液操作分离出乙酸乙酯,使用到的主要仪器为分液漏斗,因此答案是:分液;分液漏斗;
③根据流程可以知道,加硫酸能将乙酸钠转化为乙酸,且硫酸难挥发,不影响下步的蒸馏,因此正确答案是:稀硫酸;
④通过操作1得到乙酸乙酯、碳酸钠、乙酸钠、乙醇的混合液,B为乙酸、乙醇、碳酸钠的混合液,通过蒸馏得到乙醇E,然后加入稀硫酸,再蒸馏得到乙酸,因此,本题正确答案是:蒸馏;
⑤蒸馏的原理:通过控制沸点的不同来实现物质的分离,所以温度计水银球要靠近蒸馏烧瓶支管口,在蒸馏实验中除蒸馏烧瓶、温度计、冷凝管外,还需要的玻璃仪器有酒精灯、牛角管、锥形瓶;乙酸的沸点为118℃,所以收集乙酸的适宜温度是略高于118 ℃,因此答案是:b;酒精灯;冷凝管;牛角管;锥形瓶;略高于118 ℃。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】已知Ba(AlO2)2可溶于水。下图表示的是向100 mL 0.02 mol·L-1 KAl(SO4)2溶液中逐滴加入0.05 mol·L-1 Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系。下列说法不正确的是
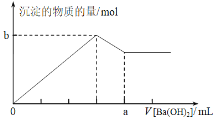
A.所加的Ba(OH)2溶液的pH=13
B.a点的值是80 mL
C.b点的值是0.005 mol
D.当V [Ba(OH)2]=30 mL时,生成沉淀的质量是0.699 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组用如图所示装置制取氯气,下列说法不正确的是
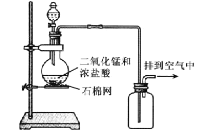
A.为了防止氯气污染空气,必须进行尾气处理
B.该装置图中存在两处明显错误
C.该实验装置中收集氯气的方法不正确
D.在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以检验是否有氯气逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中美科学家在银表面首次获得了二维结构的硼烯,该科研成果发表在顶级刊《Science》上,并获得重重点推荐。二维结构的硼烯如图所示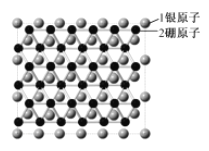 ,下列说法错误的是( )
,下列说法错误的是( )
A.1mol硼原子核外电子数为3NA
B.1molBF3分子中共价键的数目为3NA
C.1molNaBH4与水反应转移的电子数为4NA
D.硼烯有望代替石墨烯作“硼烯一钠基“电池的负极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡苯脲是一种西瓜膨大剂(植物生长调节剂),其组成结构和物理性质见下表。
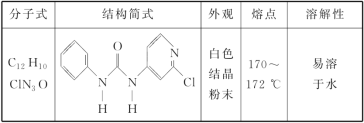
回答下列问题:
(1)氯吡苯脲晶体中,氮原子的杂化轨道类型为________。
(2)氯吡苯脲晶体中,微粒间的作用力类型有________。
A.离子键 B.金属键
C.极性键 D.非极性键
E.配位键 F.氢键
(3)查文献可知,可用2-氯-4-氨吡啶与异氰酸苯酯反应,生成氯吡脲。

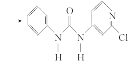
反应过程中,每生成1 mol氯吡苯脲,断裂________个σ键、断裂________个π键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。可利用太阳能光伏电池电解水制高纯氨,工作示意图如图所示。通过控制开关连接K1和K2,可交替得到H2和O2,下列有关说法错误的是( )

A.制H2时,开关应连接K1,产生H2的电极反应式是2H2O+2e-=H2↑+2OH-
B.当开关连接K2时,电极3的反应式为Ni(OH)2-e-+OH-=NiOOH+H2O
C.当开关连接K2时,电极2作阳极,得到O2
D.电极3的作用是分别作阳极材料和阴极材料,利用NiOOH和Ni(OH)2的相互转化提供电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列说法错误的是
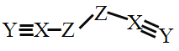
A.化合物WY是良好的耐热冲击材料
B.Y的氧化物对应的水化物可能是弱酸
C.X的氢化物的沸点一定小于Z的
D.化合物(ZXY)2中所有原子均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家采用碳基电极材料设计了一种制取氯气的新工艺方案,装置如图所示:下列说法错误的是( )

A.反应过程中需要不断补充Fe2+
B.阳极反应式是2HCl- 2e- =Cl2+2H+
C.电路中转移1 mol电子,消耗标况下氧气5.6 L
D.电解总反应可看作是4HCl(g)+O2(g)=2Cl2(g) + 2H2O(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com