
【题目】如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是( )
选项 | W | X | Y | Z |
|
A | S | SO2 | SO3 | H2SO4 | |
B | Na | Na2O2 | NaOH | NaCl | |
C | Fe | FeCl3 | Fe(OH)2 | FeCl2 | |
D | Al | AlCl3 | NaAlO2 | Al2(SO4)3 |
A.A
B.B
C.C
D.D
【答案】D
【解析】解:A.S燃烧生成二氧化硫,且S在常温下不能转化为SO3、H2SO4 , 则常温下不能发生图中转化,故A不选; B.Na燃烧生成Na2O2 , Na在常温下反应生成Na2O,则常温下不能发生图中转化,故B不选;
C.Fe燃烧生成FeCl3 , 且Fe在常温下不能直接生成Fe(OH)2 , 则常温下不能发生图中转化,故C不选;
D.Al与HCl反应生成X,Al与NaOH反应生成Y,Al与硫酸反应生成Z,Z与氯化钡反应生成X,X与NaOH反应生成Y,Y与硫酸反应生成Z,反应均可在常温下进行,故D选;
故选D.
A.S燃烧生成二氧化硫,且S在常温下不能转化为SO3、H2SO4;
B.Na燃烧生成Na2O2;
C.Fe燃烧生成FeCl3 , 且Fe在常温下不能直接生成Fe(OH)2;
D.Al与HCl反应生成X,Al与NaOH反应生成Y,Al与硫酸反应生成Z,Z与氯化钡反应生成X,X与NaOH反应生成Y,Y与硫酸反应生成Z.


科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,并用单线桥法标出电子转移的方向和数目: 。该反应中,是还原剂,是还原产物,被还原的物质是。
(2)在一定条件下,反应2NH3+3CuO ![]() 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是。
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是。
①该反应是置换反应
②反应中NH3被氧化为N2
③在反应中体现了金属铜的还原性
④在反应中每生成1 mol H2O转移1 mol电子
(3)在反应2H2S+SO2=3S+2H2O中被氧化的元素与被还原的元素的质量比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.氯化钠水溶液在电流的作用下电离出Na+和Cl-
B.硫酸钡难溶于水,但硫酸钡属于强电解质
C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
D.硫酸钠在水中的电离方程式可表示为Na2SO4=2Na++S6++4O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所述情况可能引起污染的是( )
①城市生活污水的任意排放
②农业生产中农药、化肥使用不当
③海上油轮石油泄漏
④工业生产中废液、废渣、废气的排放
A.①②
B.①④
C.②④
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W是由A、B两种元素组成的AB2型化合物.
(1)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛.则W为(填化学式).
(2)若取两支试管分别加入少量W溶液,往一支试管中滴入KSCN溶液,无明显现象. 往另一支试管中加入足量氯水,再加入适量CCl4 , 振荡,静置,下层溶液呈紫红色;往上层溶液中滴入KSCN溶液,溶液呈红色.
①W溶液中所含金属阳离子为
②上述实验中,W与足量氯水反应的离子方程式为:
(3)若W是离子化合物,其阴、阳离子均含18个电子,且阴、阳离子个数比为1:1. ①阴离子的电子式为 .
②1mol W与足量水充分反应,转移电子的物质的量为mol
(4)若A、B是同主族元素,W溶于水生成一种二元弱酸. ①B在元素周期表中的位置为
②如果A元素的周期序数是B元素的两倍,W的水溶液被双氧水氧化的化学方程式为:
(5)若如图表示0.5molW (g)和0.5mol CO(g)反应生成CO2(g)和NO(g)过程中的能量变化.则该反 应的热化学方程式为: . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3﹣0.5n]m , 广泛用于污水处理.实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO47H2O )过程如下: 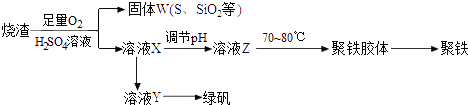
(1)验证固体W焙烧后产生的气体含有SO2的方法是 .
(2)实验室用铜和浓硫酸制备、收集干燥的SO2 , 所需仪器如下. 
装置A产生SO2 , 按气流方向连接各仪器接口,顺序为a→→→→→f,装置A中发生反应的化学方程式为 .
(3)制备绿矾时,向溶液X中加入过量 , 充分反应后,经过滤操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾.
(4)欲测定溶液Y中Fe2+的浓度,需要用容量瓶配制KMnO4标准溶液,用KMnO4标准溶液滴定时应选用(填“酸式”或“碱式”)滴定管.
(5)溶液Z的pH影响聚铁中铁的质量分数,若溶液Z的pH偏小,将导致聚铁中铁的质量分数(填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.SiO2 ![]() SiCl4
SiCl4 ![]() Si
Si
B.FeS2 ![]() SO3
SO3 ![]() H2SO4
H2SO4
C.N2 ![]() NH3
NH3 ![]() NH4Cl(aq)
NH4Cl(aq)
D.MgCO3 ![]() MgCl2(aq)
MgCl2(aq) ![]() Mg
Mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com