

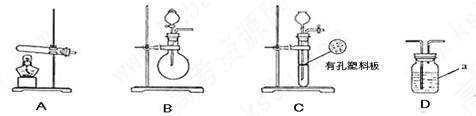
 .氧化铜反应后剩余固体的质量为
.氧化铜反应后剩余固体的质量为 .生成氮气在标准状况下的体积
.生成氮气在标准状况下的体积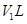 。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。
。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。 | | 实验装置 | 实验药品 | 制备原理 |
| 甲小组 | A | 氢氧化钙.硫酸铵 | 反应的化学方程式为 ① |
| 乙小组 | ② | 浓氨水.氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用: ③ |
 2NH3↑+2H2O+CaSO4(2分) ②B(1分)
2NH3↑+2H2O+CaSO4(2分) ②B(1分) NH3·H2O
NH3·H2O NH4++OH-向逆反应方向移动,加快氨气逸出(2分)
NH4++OH-向逆反应方向移动,加快氨气逸出(2分)

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
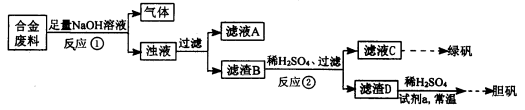
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,标况) | 1.12 | 2.24 | 3.36 | 4.48 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
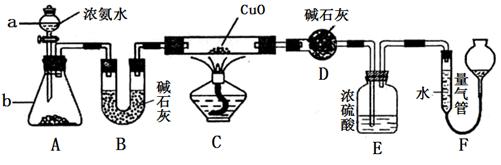
| A.Cl2与饱和食盐水 | B.CO2 与40%的NaOH溶液 |
| C.NH3与饱和食盐水 | D.HCl与水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2和O2在雷电作用下生成NO | B.某金属化合物将氮气转化为化合态氮 |
| C.在一定条件下使N2、H2合成NH3 | D.NO生成NO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
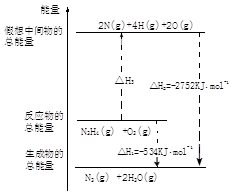
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若管道漏气遇氨就会产生白雾 | B.该反应利用了氨气的还原性 |
| C.该反应属于复分解反应 | D.生成6molNH4Cl有18mol电子转移 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Cu Cu(NO3)2 Cu(NO3)2 | B.Cu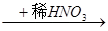 Cu(NO3)2 Cu(NO3)2 |
C.Cu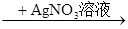 Cu(NO3)2 Cu(NO3)2 | D.Cu  CuO CuO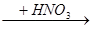 Cu(NO3)2 Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com