
����Ŀ���뼰�仯�����Ӧ�������汻���ӡ�
��l������Ҫ�ĺ������������ʯ����2������Cr��������ʯ��Ϊ��ĸ�̡���̬Crԭ�Ӽ۵��ӵĹ����ʾʽΪ_____________________��
��2�����������������Ԫ���������ơ������й��������������ȷ����_______�����ţ���
A��������p������Ԫ�� B���縺�Զ���þ��
C����һ�����ܶ���þ�� D.�Ȼ����ˮ��ҺpH��С��7
��3���롢�����嶼���ɽ���ԭ�����ò�����ά�ռ�ѻ����ɣ����ܶѻ���������۵�(155lK)�������۵�(930K)�ߣ�ԭ����__________________________��
��4���Ȼ�������̬ʱ����BeC12���ӣ�a���Ͷ��۷��ӣ�BeCl2)2(b)����̬ʱ���������ͼ��ʾ����״�ṹ��c����

��a����__________������ԡ��Ǽ��ԡ������ӡ�
�ڶ��۷��ӣ�BeCl2)2��Beԭ�ӵ��ӻ���ʽ��ͬ��������ԭ�Ӷ���ͬһƽ���ϡ�b �ĽṹʽΪ________________________________ �������λ������
��c��Beԭ�ӵ��ӻ���ʽΪ__________��
���Ȼ��뾧���д��ڵ���������_____�����ţ���
A�����»��� B. �Ҽ� C.���Լ� D���Ǽ��Լ� E�����Ӽ�
��5��BeO������������ͼ��ʾ��

��BeO������ܶ�Ϊdg/cm3��������a =______nm ���г�����ʽ���ɣ���
���𰸡� ![]() B��D Beԭ�Ӱ뾶��Alԭ�Ӱ뾶С�������Ը�ǿ �Ǽ���
B��D Beԭ�Ӱ뾶��Alԭ�Ӱ뾶С�������Ը�ǿ �Ǽ��� ![]() sp3 A��B��C
sp3 A��B��C ![]()
��������(l)Crԭ��Ϊ24��Ԫ�أ������������ȫ�����ȶ��ṹ����̬ԭ�Ӽ۲�����Ų�ʽΪ3d54s1,���̬Crԭ�Ӽ۵��ӵĹ����ʾʽΪ![]() ��
��
(2)A��������s��Ԫ�أ���������p������Ԫ�أ���A����B������Խ���ã������ԽС��Mg��Be��Al���ã����������縺�Զ���þ��B��ȷ��C��Be�ĵ�һ�����ܱ�þ��Mg��s���ȫ��������һ�����ܱ�Al��C����D.Be2+��Al3+����Һ�о�ˮ�⣬���Ȼ����ˮ��ҺpH��С��7����D��ȷ����ΪBD��
(3)��ΪBeԭ�Ӱ뾶��Alԭ�Ӱ뾶С�������Ը�ǿ��������۵�������۵����
(4)�Ȼ�������̬ʱ����BeC12����(a)�Ͷ��۷���(BeCl2)2(b)����̬ʱ���������ͼ��ʾ����״�ṹ(c)��
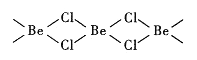
��BeCl2��Beԭ�ӳ�2��Be-Cl��Beԭ�ӵ��ӻ������Ϊ2����Beԭ�Ӳ�ȡsp�ӻ���ʽ����ֱ���ͣ����ڷǼ��Է�����
���ڶ��۷���(BeCl2)2��Beԭ���пչ����Clԭ���й¶Ե��ӣ�����λ���е��Ӷ�����ԭ���ṩ��b �ĽṹʽΪ![]() ��
��
������пչ�����Ⱦ��йµ��Ӷԣ����Զ����(BeCl2)N�ṹ��ͼΪ![]() �м۲���ӶԸ���=4������ԭ������sp3�ӻ���
�м۲���ӶԸ���=4������ԭ������sp3�ӻ���
�� �Ȼ��뾧���Ƿ��Ӿ��壬���Ӽ��з��»�������������Be��Cl���Լ���Ҳ�������������ڷǼ��Լ������Ӽ����ʴ�ΪABC��
(5)BeO����������ͼ��ʾ������Be2+��ĿΪ4��O2-��ĿΪ8![]() +6��
+6��![]() =4�������к���4��BeO������������Ϊ
=4�������к���4��BeO������������Ϊ![]() g���辧���ı߳�Ϊanm���������Ϊ(a��10-7)3cm3���������ܶ�dg/cm3=
g���辧���ı߳�Ϊanm���������Ϊ(a��10-7)3cm3���������ܶ�dg/cm3=![]() g��(a��10-7)3cm3����a=
g��(a��10-7)3cm3����a=![]() nm��
nm��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ�����ʲô�����Ȼ�ϣ�ֻҪ����������һ�������ȼ��ʱ������ˮ������Ϊ��ֵ������������
A. C2H2��C6H6B. C2H2��C4H6C. C2H4��C4H10D. C6H6��C7H8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���Ӧ����ͬһ���͵��ǣ� ��
A. ������һ�ȼ��顢���������� B. �����屽����ϩ���Ҵ�
C. �Ҵ�����ȩ���Ҵ����������������� D. ��ϩ�ƾ���ϩ����ȩ��֬���Ʊ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ����( )
A. ��ԭ�ӵļ۵����Ų�ͼ��![]()
B. �۵����Ų�Ϊ4s24p3��Ԫ��λ�ڵ������ڵڢ�A�壬��p��Ԫ��
C. 2p��3p�����״��Ϊ�����Σ�����Ҳ���
D. ��ԭ����1s22s22p63s1��1s22s22p63p1ʱ��ԭ���ͷ��������ɻ�̬ת���ɼ���̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ������ͼ���dz��õĿ�ѧ�о�������
(1)������ij����Ԫ��M�ĵ����������ͼ1��ʾ����MԪ��λ�����ڱ��ĵ�________�塣

(2)ͼ2���о���������Ԫ���⻯��ķе�仯���ɵ�ͼ������c���Ա������________��Ԫ����̬�⻯��ķе�仯���ɡ���λͬѧ��ij����Ԫ���⻯��ķе�ı仯���ƻ������������ߣ�a��b��������Ϊ��ȷ��������___________����a��b����
(3)���ֶ���������Ԫ�ص�����������Ӧ��ˮ���Ũ�Ⱦ�Ϊ0.01mol.L-1)��Һ��pH��ԭ�������Ĺ�ϵ����ͼ��ʾ��Ԫ��R�����ڱ��е�λ����______________��Ԫ��Y��ԭ�ӽṹʾ��ͼ��____________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��WΪԪ�����ڱ�ǰ�����ڵ�Ԫ�ء�����X���γɻ�������������Ԫ�أ�Y���ڲ��������������������9����Z��Ԫ�����ڱ��е縺������Ԫ�أ�WԪ�صĵ������Ӳ㴦��ȫ����״̬�ҵ��ĵ��Ӳ�ֻ��2�����ӡ���ش��������⡣
(1)WԪ����Ԫ�����ڱ��е�λ��Ϊ______________________________��
(2)W2�����백�������γ�������[W(NH3)4]2����д���������ӵĽṹ��ʽ(������λ��)_______��
(3)X�����⡢����������Ԫ�ع��ɻ�����XO(NH2)2������Xԭ�ӵ��ӻ���ʽΪ__________��1mol�÷����ЦҼ�����ĿΪ______________��������������ˮ����Ҫԭ����________________��
(4)X��ij�־���Ϊ��״�ṹ���������ڽ��������á���ԭ������ڸ���֮�䣬�γɼ�϶������䳣���ṹ��ƽ��ͶӰ��ͼ����ʾ�����仯ѧʽ�ɱ�ʾΪ______________________��
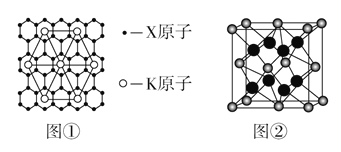
(5)Ԫ��Y��Ԫ��Z�γɵľ����ṹ��ͼ����ʾ���þ�����Y������Χ�����Z������Ϊ___����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ��ѡ��3�����ʽṹ������]
��п��ZnS���������������Լ���ӫ���塢���ģ�����ʪ�������ױ�����ΪZnSO4���ش��������⣺
��д����̬Znԭ�ӵļ۵����Ų�ʽ__________����̬Sԭ�Ӻ���δ�ɶԵ�����Ϊ_____��
��ZnSO4������Ԫ�صĵ縺���ɴ�С��˳��Ϊ_____________________��SO42�������幹��Ϊ________________������S���ӻ��������Ϊ_________��
������п���ڰ�ˮ������[Zn(NH3)4]SO4��Һ��[Zn(NH3)4]SO4��Һ�������ڵ�������������___________��
a.���Ӽ� b.���ۼ� c.��λ�� d.���»��� e.���
�ȸ�������п±������۵���ܽ��ԣ��ж�ZnF2���������Ϊ___________������ZnCl2��ZnBr2��ZnI2�۵����������ԭ��________________��
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
�۵�/�� | 872 | 275 | 394 | 446 |
���Ҵ����������ܽ��� | ���� | �ܽ� | �ܽ� | �ܽ� |
������ZnS������ܶ�Ϊ��g��cm-3���侧���ṹ��ͼ��S2����Χ�Ⱦ����������Zn2+��S2������Ϊ______��______��ZnS�����еľ�������a=________nm(�г�����ʽ)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(H3BO3)��һ��Ƭ��״�ṹ��ɫ���壬���ڵ�H3BO3����ͨ���������(����ͼ)�������й�˵����ȷ����

A. ��H3BO3�����и�ԭ�������ȫ������8�����ȶ��ṹ
B. H3BO3���ӵ��ȶ���������й�
C. 1mol H3BO3�ľ�������3mol���Թ��ۼ�
D. 1mol H3BO3�ľ�������3mol���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֲ�ͬ�ѻ���ʽ�Ľ�������ľ�����ͼ��ʾ���й�˵����ȷ����( )

A. ��Ϊ�������ѻ� ��Ϊ�������ܶѻ� ��Ϊ���������ѻ� ��Ϊ�����������ܶѻ�
B. ÿ���������е�ԭ�����ֱ�Ϊ����1������2������2������4��
C. ������ԭ�ӵ���λ���ֱ�Ϊ����6����8����8����12
D. �ռ������ʵĴ�С��ϵΪ����������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com