
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.分析 (1)溴乙烷沸点低,溴乙烷易挥发,用水浴加热热均匀,减少溴乙烷的损失;
(2)溴乙烷不溶于水,开始溶液分层,生成物乙醇、溴化钠都溶于水;
(3)根据乙醇分子结构中有三种氢原子选择检测方法;
(4)溴乙烷在NaOH乙醇溶液中发生消去反应,生成乙烯,乙烯能够使酸性的高锰酸钾褪色(或者使溴的四氯化碳褪色),只要证明乙烯的存在即可证明发生的是消去反应.
解答 解:(1)溴乙烷沸点低,溴乙烷易挥发,用水浴加热热均匀,减少溴乙烷的损失,
故答案为:使试管受热均匀,减少溴乙烷的损失;
(2)溴乙烷不溶于水,开始溶液分层,生成物乙醇、溴化钠都溶于水,当溶液分层消失,表明溴乙烷与NaOH溶液已完全反应,
故答案为:溶液分层消失;
(3)乙醇分子结构中有三种氢原子,它们的比为3:2:1,利用核磁共振氢谱可检测,也可用红外光谱检测,
故答案为:核磁共振氢谱或红外光谱;
(4)溴乙烷在NaOH乙醇溶液中发生消去反应,生成乙烯,只有证明乙烯的存在即可证明发生的是消去反应,所以需要检验的是生成的气体,方法是:将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,酸性KMnO4溶液褪色(或直接通入溴的四氯化碳溶液,四氯化碳褪色),
故答案为:生成的气体;将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,酸性KMnO4溶液褪色(或直接通入溴的四氯化碳溶液,四氯化碳褪色).
点评 考查卤代烃的性质、反应原理的探究、对实验装置的理解等,难度不大,注意(1)中取代反应实质是,溴乙烷与是发生取代反应生成乙醇与氢溴酸,氢溴酸与氢氧化钠反应生成溴化钠与水,所以还发生中和反应.


科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①② | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
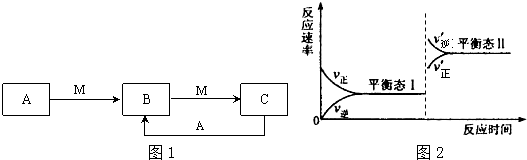
 已知A、B、C是单质且C是绿色植物光合作用的产物之一,X、Y是化合物,它们之间的转化关系如图(反应条件略).下列A、B间的对应关系,不正确的是( )
已知A、B、C是单质且C是绿色植物光合作用的产物之一,X、Y是化合物,它们之间的转化关系如图(反应条件略).下列A、B间的对应关系,不正确的是( )| A. | A是镁,B是碳 | B. | A是碳,B是氢气 | C. | A是铝,B是铁 | D. | A是钠,B是氢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2).已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成.有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,CO2无强还原性,反应原理不相同.据此设计如下实验操作进行判断.
过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2).已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成.有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,CO2无强还原性,反应原理不相同.据此设计如下实验操作进行判断.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
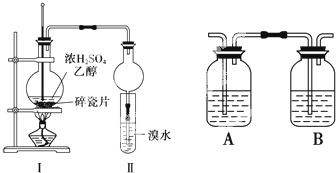 某化学兴趣小组用如图所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.
某化学兴趣小组用如图所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )
关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )| A. | ①②③ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com