
| A、C1>C2 |
| B、C1=C2 |
| C、C1<C2 |
| D、2 C1=C2 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16O2与18O2互为同素异形体 |
| B、16O与18O是氧元素的两种核素 |
| C、通过化学变化可以实现16O与18O间的相互转化 |
| D、16O与18O核外电子排布方式不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,1mol任何物质的体积约为22.4L |
| B、非标准状况下,1mol任何气体的体积不可能为22.4L |
| C、1mol氖气和1mol氧气体积相同 |
| D、标准状况下,1mol氧气和氮气(任何比混合)的混合气的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可用丁达尔现象区别 |
| B、加入硫酸镁溶液前者会浑浊而后者无明显现象 |
| C、可用渗析的方法分离 |
| D、可用过滤的方法分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、绿色食品就是指颜色为绿色的食品 |
| B、白色污染是指白色的废弃物的污染 |
| C、有机食品是指含有有机物的食品 |
| D、含有羧基的有机物能发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
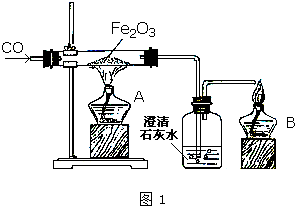 某研究性学习小组在用右图装置进行CO还原Fe2O3的探究实验.
某研究性学习小组在用右图装置进行CO还原Fe2O3的探究实验.| 实验编号 | 实 验 操 作 | 实 验 现 象 |
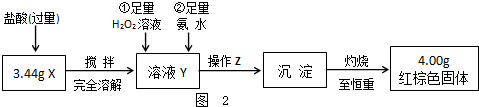
| ① | 取少量黑色粉末X放入试管1中,注入适量稀盐酸,微热. | 黑色粉末逐渐溶解, 有无色气体逸出. |
| ② | 向试管1所得溶液中滴加几滴 KSCN溶液,振荡. | 溶液未出现血红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com