
【题目】常温下,下列粒子浓度关系错误的是
A. 0.1 mol·L-1CH3COONa溶液中:c(Na+)>c(OH-)>c(CH3COOH)>c(H+)
B. pH=5的CH3COOH和CH3COONa混合溶液中:c(CH3COO-)>c(Na+)
C. 将0.2mol·L-1CH3COOH溶液与0.1mo1·L-1NaOH溶液等体积混合:c(CH3COO一)+c(CH3COOH) = 2c(Na+)
D. 向0.10mol·L-1NH4HCO3溶液中通入CO2至中性:c(NH4+) = c(HCO3-)+ c(CO32-)
【答案】D
【解析】A.根据CH3COO-+H2O![]() CH3COOH+OH-和H2O
CH3COOH+OH-和H2O![]() H++OH-,CH3COONa溶液呈碱性,且c(OH-)略大于c(CH3COOH),因此c(Na+)>c(OH-)>c(CH3COOH)>c(H+),故A正确;B. pH=5的CH3COOH和CH3COONa混合溶液显酸性,说明乙醋酸的电离为主,则c(CH3COO-)>c(Na+),故B正确;C. 将0.2mol·L-1CH3COOH溶液与0.1mo1·L-1NaOH溶液等体积混合恰好形成等物质的量浓度的醋酸和醋酸钠的混合溶液,根据物料守恒c(CH3COO一)+c(CH3COOH) = 2c(Na+),故C正确;D. 向0.10mol·L-1NH4HCO3溶液中通入CO2至中性,根据电荷守恒,c(NH4+) + c(H+)= c(HCO3-)+2c(CO32-)+ c(OH-),由于c(OH-)=c(H+),则c(NH4+) = c(HCO3-)+2c(CO32-),故D错误;故选D。
H++OH-,CH3COONa溶液呈碱性,且c(OH-)略大于c(CH3COOH),因此c(Na+)>c(OH-)>c(CH3COOH)>c(H+),故A正确;B. pH=5的CH3COOH和CH3COONa混合溶液显酸性,说明乙醋酸的电离为主,则c(CH3COO-)>c(Na+),故B正确;C. 将0.2mol·L-1CH3COOH溶液与0.1mo1·L-1NaOH溶液等体积混合恰好形成等物质的量浓度的醋酸和醋酸钠的混合溶液,根据物料守恒c(CH3COO一)+c(CH3COOH) = 2c(Na+),故C正确;D. 向0.10mol·L-1NH4HCO3溶液中通入CO2至中性,根据电荷守恒,c(NH4+) + c(H+)= c(HCO3-)+2c(CO32-)+ c(OH-),由于c(OH-)=c(H+),则c(NH4+) = c(HCO3-)+2c(CO32-),故D错误;故选D。


科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 碳酸氢钠溶液与盐酸反应: CO32-+2H+===CO2↑+H2O
B. 氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH-![]() H2O+NH3↑
H2O+NH3↑
C. 氢氧化镁与稀硫酸反应:H++OH-===H2O
D. 单质铜与稀硝酸反应:Cu+2H++2NO3-===Cu2++2NO↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验浓硫酸与木炭在加热条件下反应产生SO2和CO2气体,设计了下图实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用酸性高锰酸钾溶液浸湿的脱脂棉。

请回答下列问题:
(1)实验前需进行的操作是_______________________________
(2)写出圆底烧瓶中所发生的反应方程式____________________________________________
(3)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是________(用编号填写);
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(4)实验时,装置C中的现象为______________
(5)当D中产生______(用字母填写)现象时,可以说明使E中澄清石灰水变浑的是CO2,而不是SO2;
A.进气口一端脱脂棉紫色变浅,出气口一端脱脂棉紫色不变
B.脱脂棉上紫色均变浅 C.脱脂棉上紫色褪去
则装置D的作用为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.1mol·L-1HF溶液中加入0.1 mol CaCl2固体(不考虑溶液体积变化),则下列说法中错误的是
A. 原HF溶液c(H+)约为6×10-3mol·L-1
B. 加入 CaCl2后溶液中有CaF2沉淀产生
C. 加入CaCl2后溶液中的c(H+)浓度不变
D. 2HF(aq)+Ca2+(aq)=CaF2(s)+2H+(aq)的平衡常数为K=8.88×102
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种白色晶体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。通常利用CaCl2在碱性条件下与H2O2反应制得。某化学兴趣小组在实验室制备CaO2的实验方案和装置示意图(图一)如下:


已知:CaO2的制备原理:CaCl2+H2O2+2NH3H2O+6H2O= CaO28H2O↓+2NH4Cl
请回答下列问题:
(1)仪器C的名称为__________,支管B的作用____________;
(2)加入氨水的作用是_______;(从化学平衡移动的原理分析)
(3)过滤后洗涤沉淀的试剂最好用_______;
A.水 B.浓盐酸 C.无水乙醇 D.CaCl2溶液
(4)沉淀反应时常用冰水浴控制温度在O℃左右,其可能原因是_________、_______(写出两种)。
(5)已知CaO2在350℃时能迅速分解,生成CaO和O2。该小组采用如图二所示的装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)
①检查该装置气密性的方法是:________________;
②准确称取0.50g样品,置于试管中加热使其完全分解,收集到44.80mL(已换算为标准状况)气体,则产品中过氧化钙的质量分数为________(保留4位有效数字);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴是小组对一种度旧合金(含有Cu、Fe、Si等元素)进行分离、回收利用,所设计工艺流程如下。
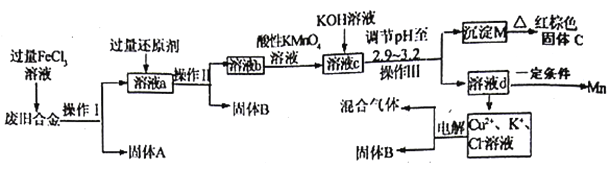
已知298℃时,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Mn(OH)2]=1.9×10-13,当离子浓度小于1×10-5认为离子沉淀完全。
回答下列问题:
(1)操作I、lI、III为_______,固体A是__________(填化学式)。
(2)加入过量FeC13溶液过程中与较不活泼的金属反应的化学方程式_______。
(3)调节pH至2.9--3.2的目的___________________。
(4)①向溶液b中加入酸性KMn04溶液发生反应的离子方程式为_________________。
②若将溶液b配制成250ml溶液,用滴定管取配制后的溶液25.00m1;再用amol/LKMnO4溶液滴定,恰好反应时消耗KMn04溶液VmL,则流程图中所得红棕色固体C的质量为___g(用含a、v的代数式表示)
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶液,最后沉淀的金属离子为____________(填金属阳离子)。
(6)用惰性电极电解(Cu2+、K+、C1-溶液)一段时间后,阴、阳两极均产生标准状况下的气体6.72L,阴极析出固体3.2g,则原溶液C1-的物质的量为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是基本有机化工原料,由乙炔制备聚乙烯醇和顺式聚异戊二烯的合成路线(部分反应条件略去)如图所示:
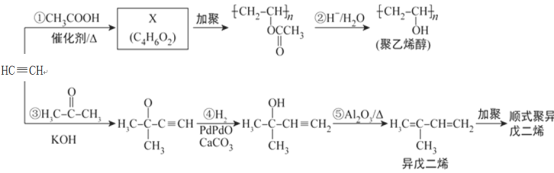
回答下列问题:
(1)按系统命名法命名异戊二烯:________________________________________。
(2)X分子中含有的官能团名称是________________________________________。
(3)反应①~③中,__________(填反应序号)的反应类型与反应④不同,反应⑤属于__________反应。
(4)与乙炔具有相同官能团的异戊二烯的同分异构体共有__________种。
(5)X的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是__________(选填字母)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
(6)顺式聚异戊二烯的结构式是(选填字母)__________。
a.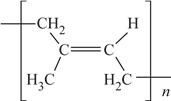 b.
b.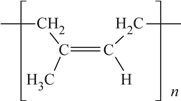
c.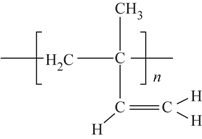 d.
d.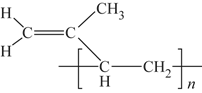
(7)参照异戊二烯的上述合成路线,设计一条由乙烯和乙醛为起始原料制备1,3-丁二烯的合成路线:_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用稀硝酸与铜反应制备NO气体,如果采用图Ⅰ装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不是十分理想,因为观察到的现象不能有力证明反应产物是NO。有人设计了图Ⅱ装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果。
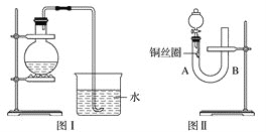
(1)用图Ⅰ装置做实验时,用排水法收集到的气体的颜色为_____色;实验过程中由于______,不易观察到____________生成,从而不能有力证明反应产物是NO。
(2)用图Ⅱ装置做实验时,将有关操作补充完全:
①将分液漏斗的活塞打开,从U形管的B侧管口注入稀硝酸,一直注到____________为止。
②关闭活塞,用酒精灯在U形管的A侧加热,当______时,立即撤去酒精灯。
(3)根据图Ⅱ装置的实验完成下列问题:
①反应在什么情况下可以自动停止?________________________。
可在何处观察到无色的NO气体?____________________________________________。
②如果将分液漏斗的活塞慢慢打开,可立即观察到哪些明显现象?_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com