
【题目】向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s) ![]() yC(g) ΔH<0,一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
yC(g) ΔH<0,一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
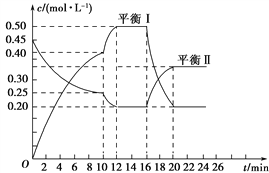
(1)用A的浓度变化表示该反应在0~10 min内的平均反应速率v(A)=______________________。
(2)根据图示可确定x∶y=________。
(3)0~10 min容器内压强________(填“变大”、“不变”或“变小”)。
(4)推测第10 min引起曲线变化的反应条件可能是______________________;第16min引起曲线变化的反应条件可能是________________________。
①减压 ②增大A的浓度 ③增大C的量 ④升温⑤降温 ⑥加催化剂
(5)若平衡Ⅰ的平衡常数为K1,平衡Ⅱ平衡常数为K2,则K1________K2(填“>”、“=”或“<”)。
【答案】 0.02mol/L 1:2 变大 ④⑥ ④ >
【解析】试题分析:(1)0~10min内容器中A的物质的量浓度变化为:0.45mol/L-0.25mol/L=0.2mol/L;0~10min内容器中C的物质的量浓度变化为:0.40mol/L,x:y=0.2mol/L:0.40mol/L=1:2。
(2)0~10min内△n(A)=0.45mol-0.25mol=0.2mol,v(A)=△c/△t=[(0.450.25)mol/L]÷10min=0.02mol·(L·min)-1。
(3)反应前气体物质的量小于反应后气体物质的量,随着反应的进行,气体物质的量增大,气体压强增大。
(4)第10min时,单位时间内A、C的物质的量变化量较大,反应速率明显增大,可能为升高温度或者使用催化剂;第16min时,C的物质的量减小,A的物质的量增大,说明平衡向逆反应方向移动,该反应为放热反应,应为升高温度。
(5)已知第16min时改变的条件是升高温度,而该反应是放热反应,所以升高温度平衡逆移,则平衡常数减小,所以K1>K2。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】实验室制取下列气体,所用药品正确的是 ( )
A. 用碳酸钙与稀硫酸反应制取CO2
B. 用H2O2溶液和MnO2制取O2
C. 用铁与浓硫酸反应制取氢气
D. 用氯化铵加热分解制取氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某强酸性溶液 X 中含有 Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、 NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:

根据以上信息,回答下列问题:
(1) 上述离子中,不能确定是否含有的离子是_______________,若要用实验证明该离子一定不存在,最可靠的化学方法是______________________。
(2)写出下列反应的关离子方程式:
①中生成气体A:_______________________。
②生成沉淀I:____________________________。
(3)假设测定A、F、I均为0.01mol,10mLX溶液中n(H+)=0.04mol,且不能确定含有的离子只有一种,当X溶液中不能确定的离子是__________,沉淀C的物质的量为______________。
Ⅱ.辉铜矿的主要成分是Cu2S,从辉铜矿中浸取铜元素,可用FeCl3作浸取剂。
(1)浸取时的反应为:Cu2S+4FeCl3=2CuCl2+4FeCl2+S,浸取过程中加入洗涤剂溶解硫时,铜元素的浸取率的变化如图。其原因是_________________。

353K时,向FeCl3浸取液屮加入CuCl2,能加快铜元素的浸取速率,其反应原理可用化学方程式表示为_______________, CuCl+FeCl3=CuCl2+FeCl2。
(2)CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。试确定200℃时固体物质的化学式为__________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+3B(g)=2C(g)+D(g),经2min,B的浓度减少0.6mol·L-1。对此反应速率的表示,正确的是
①用A表示的反应速率是0.4 mol·L-1·min-1 ②分别用B、C、D表示的反应速率其比值为3∶ 2∶1 ③在2 min末的反应速率,用B表示是0.3mol·L-1·min-1④在这2 min内用B表示的反应速率的值是逐渐减小的,用C表示的反应速率的值是逐渐增大的( )
A. ①② B. ③ C. ① D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】符合如图所示的转化关系,且当X、Y、Z的物质的量相等时,存在焓变△H=△H1+△H2。满足上述条件的X、Y可能是

①C、CO ②S、SO2 ③Na、Na2O ④AlCl3、Al(OH)3 ⑤Fe、Fe(NO3)2 ⑥NaOH、Na2CO3
A. ①④⑤ B. ①②③ C. ①③④ D. ①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石墨棒作电极,电解CuCl2溶液,若电解时转移的电子数是3.01×1023,则此时在阴极上析出的的铜的质量是
A.8gB.16gC.32gD.64g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H<0
CO2(g)+H2(g) △H<0

下列分析中正确的是
A、图Ⅱ研究的只是t0时使用催化剂对反应速率的影响
B、图Ⅰ研究的是t0时缩小容器体积对反应速率的影响
C、图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
D、图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿泉水瓶上标有:钙>4.0mg/mL,钠>30.00 mg/mL,这里的“钙”、“钠”指的是( )
A. 原子 B. 分子 C. 元素 D. 单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com