
| 选项 | A | B | C | D |
| 实验 操作 | 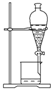 | 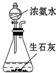 | 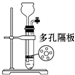 | 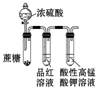 |
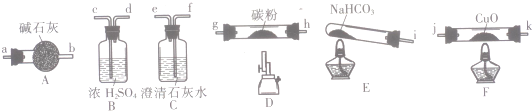
| 实验 目的 | 分离乙酸与乙酸乙酯的混合液 | 制取氨气 | 盐酸与碳酸钙反应,验证碳与氯的非金属性强弱 | 验证浓硫酸具有脱水性、强氧化性,SO2具有漂白性、氧化性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.互溶的液体应该采用蒸馏方法分离提纯,互不相溶的液体采用分液方法分离;
B.浓氨水与生石灰反应可以制取氨气;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
D.二氧化硫具有还原性,能被强氧化剂氧化.
解答 解:A.乙酸、乙酸乙酯是互溶的,不能用分液漏斗分离,应该采用蒸馏方法分离,故A错误;
B.CaO和水反应生成氢氧化钙且放出热量,放出的热量导致一水合氨分解,所以浓氨水与生石灰反应可以制取氨气,故B正确;
C.盐酸和碳酸钙反应生成二氧化碳和水,说明盐酸酸性大于碳酸,因为HCl不是Cl元素的最高价氧化物的水化物,所以该实验不能判断非金属性强弱,故C错误;
D.SO2被酸性高锰酸钾反应氧化而使酸性高锰酸钾溶液褪色,该实验体现SO2具有还原性,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及物质分离和提纯、气体制备、非金属性强弱判断、二氧化硫的性质等知识点,侧重考查学生分析及知识综合运用、实验操作能力,易错选项是C,把握物质性质是解本题关键,易错选项是C.


科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅可用于制造光导纤维 | |
| B. | 石英玻璃可用于制造光学仪器 | |
| C. | 玻璃在加热融化时有固定的熔点 | |
| D. | 制普通玻璃的原料是纯碱、石灰石、石英 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽车尾气中的CO﹑NO等都是大气污染物 | |
| B. | 氢键﹑离子键﹑共价键都是微粒间的作用力,且属于化学键 | |
| C. | 高压钠灯发出的黄光射程远,透雾能力强,常用于道路和广场的照明 | |
| D. | 用食醋可以除去热水壶内壁的水垢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 操作 | 现象 |
| a | 加入足量稀硝酸、振荡 | 试管内红色固体完全溶解,溶液变为蓝色,并有无色气体产生 |
| b | 加入足量稀硫酸、振荡 | 试管内有红色固体,溶液为无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
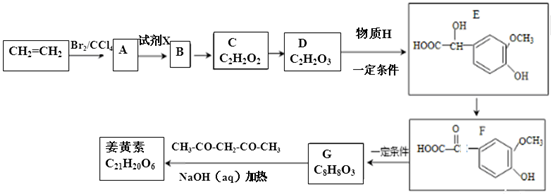
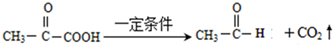
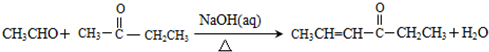
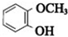 .
. .
.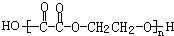 +(2n-1)H2O.
+(2n-1)H2O.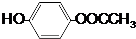 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
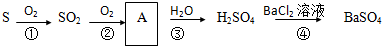
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL、1 mol.L-1的AlCl3溶液中,含Al3+的数目为0.1 NA | |
| B. | 1mol 羟基中所含的电子数为10NA | |
| C. | 2L0.5mol/L亚硫酸溶液中含有的H+离子数为2NA | |
| D. | 2.8 g乙烯与一氧化碳的混合气体,所含分子数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高正化合价:F>O>N>C>Al | B. | 离子半径:F->O2->Na+>Al3+ | ||
| C. | 热稳定性:PH3<H2S<HCl<HF | D. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3>KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期零族 | B. | 第四周期第IIA族 | C. | 第三周期第ⅠA族 | D. | 第三周期第ⅦA族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com